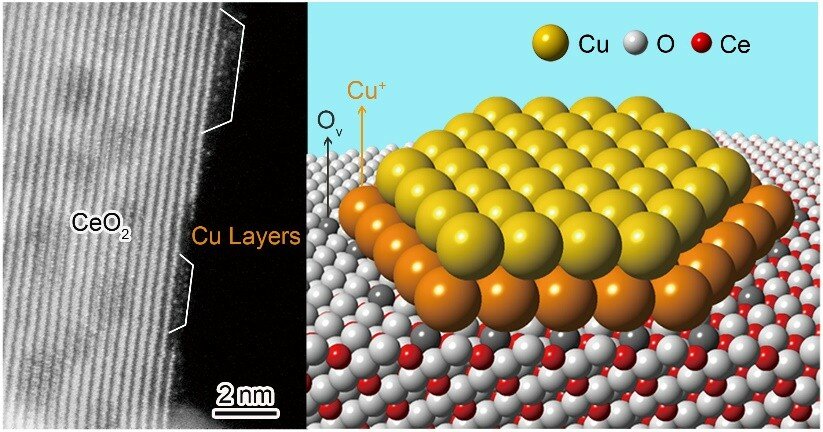
تحديد التركيب الذري للطبقة السطحية في حفازات (النحاس – السيريوم)، فلقد تمكّن مؤخراً الدكتور (زهو يان – Zhou Yan)، والأستاذة البروفيسورة (شين وينجي – Shen Wenji) من معهد (داليان للفيزياء الكيميائية – The Dalian Institute of Chemical Physics = DICP) التابع للأكاديمية الصّينية للعلوم، ومعاونيهم من تحديد التركيب الذّري للطّبقة السّطحية للحفّاز الكيميائي النّشط (نحاس – سيريوم / Cu–CeO2)، كما اقترحوا نموذجًا لعنصر النّحاس ثنائي الطّبقة، وقد نُشرت هذه النتائج التي توصلوا إليها في مجلة (Nature Catalysis).
تحديد التركيب الذّري لعنصر النّحاس ثنائي الطّبقة
ولكن، في الحقيقة، ونظرًا للوفرة الطّبيعية، التكُّلفة المنخفضة، والأهم من ذلك بسبب خصائصها الإلكترونية الفريدة، فقد تمّ استخدامُ حفّازات النّحاس في التّطبيقات الصّناعية، ودراستها بشكلٍ أساسي للعديد من التفاعلات الكيميائية التي ترتبط بمجال الطاقة.
وتتشكل جسيمات النّحاس النانوية المتبعثرة فوق سطح عنصر السيريوم (Ce)، ولكن، نظاماً مُحفّزاً عاليَ الكفاءة لتفاعل الحصول على “غاز الماء/Water-Gas ” في درجات الحرارة المنخفضة وهو ما يعرف بـِ (WGS = The low-temperature Water–Gas shift)، والذي يُعطي عنصر الهيدروجين (H2) و “أول أكسيد الكربون/ثاني أكسيد الكربون (CO/CO2)” المهدرج؛ وهذا الأخير يعطي بدوره الميثانول (الكحول الميتيلي)، وهنا تكمن أهمية هذا التفاعل في استثمار واستخدام مصادر الكربون.
ولكن، الجدير بالذكر أنّ “غاز الماء” الذي يتم صناعته عن طريق تفاعل تحويل الماء إلى غازٍ يُساهم في استخلاص الهيدروجين النّقي (أو على الأقل الهيدروجين المخصّب)؛ حيث يتفاعل أول أكسيد الكربون الناتج عن التفاعل الأولي مع الماء ليؤدي إلى إزالة ثاني أكسيد الكربون، تاركًا فقط غاز الهيدروجين، ولكن، هنا يجب الانتباه إلى التعامل معه بحذر بسبب خطر التّسمم بأول أكسيد الكربون.
ولكن، بحسب الدراسة فإنّ السّطح الفاصل بين النّحاس والسيريوم هو المسؤول عن الأداء المميز للحفّاز؛ وبالرغم من ذلك، لا يزال هناك الكثيرُ من التّحديات للكشف المباشر والتوصيف الكمّي للمواقع المسؤولة عن عملية التنشيط هذه للتفاعل بواسطة الحفّاز (نحاس – سيريوم).
يمكنك أيضًا الأطلاع على: تحول اللوحات التاريخية من اللون الأخضر إلى البني ودور خلات النحاس في ذلك
حفازات (النحاس – السيريوم)
وقد صرّحت الأستاذة البروفيسورة (شين) قائلةً:
” نحن نستندُ في استنتاجاتنا إلى ملاحظة مجموعاتٍ من العناقيد النّحاسية الصغيرة عن طريق:
- الجمع بين الجهاز المجهري لمسح النفاذية الإلكترونية (A Scanning Transmission Electron Microscope = STEM).
- وجهاز التّحليل الطّيفي لحساب ضياع الطّاقة الإلكترونية (Electron Energy Loss Spectroscopy = EELS ).
- بالإضافة إلى تحليل بيئة الترابط البيني باستخدام التحليل الطيفي للأشعة تحت الحمراء (IR).
- وأخيراً حسابُ معدل الكثافة باستخدام نظرية معامل الكثافة الوظيفي (Density Functional Theory = DFT).
وأضافت البروفيسورة (شين) أيضاً:
“لقد وجدنا عند دراسة التركيب الذّري لسطح الحفّاز أنّ:
- البنية الذّرية النّحاسية مؤلفةٌ من طبقةٍ سفليةٍ من أيونات النّحاس الموجبة (Cu+) .
المرتبطة بمواقع ذرات الأكسجين الشاغرة، والناتجة عن مركب رباعي أكسيد السريوم (CeO₂)، وطبقة عليا من أكسيد النحاس (CuO) المتوافقة مع أيونات شاردة النحاس الموجبة (Cu+).”
علاوةً على ذلك، وجدَ العلماءُ أنّ:
- تفاعل “غاز الماء – WGS” قد جرى على السطح البيني للحفّاز الكيميائي (النحاس-السيريوم).
- وذلك من خلال آلية التشاركية في الموقع.
حيث يقوم موقع شاردة النّحاس الموجبة (Cu+) بامتصاص ثاني أكسيد الكربون (CO2) كيميائيًا، بينما تَنْشُط في ذات الوقت المواقع المجاورة لذرات الأكسجين الشاغرة مما يٌساهم في تنشيط عملية فصل الماء.
المصادر:
Aling Chen et al, Structure of the catalytically active copper–ceria interfacial perimeter, Nature Catalysis (2019). DOI: 10.1038/s41929-019-0226-6
Water Gas Definition and Uses. ThoughtCo. Retrieved December 4, 2019, from https://www.thoughtco.com/definition-of-water-gas-605785
Scientists identify atomic structure of catalytically active copper-ceria interface. EurekAlert. Retrieved December 4, 2019, from https://www.eurekalert.org/pub_releases/2019-02/caos-sia021719.php