أفكار يجب أن تموت في تعليم الكيمياء: المجموعة الثالثة

ألهمني كتاب “هذه الفكرة يجب أن تموت” بهذه السلسلة من المقالات وفي هذا الكتاب يشرح 175 مفكر بارز مجموعة من الأفكار، والنظريات والمفاهيم التي يعتقدرون أنها أصبحت غير مثمرة ويجب التخلي عنها، وخصوصا في ترتيب المجموعة الثالثة للعناصر بالجدول الدوري، ومما لفت نظري أنه لم يشارك أي كيميائي في هذا الكتاب.
افتقاد الكيمياء للمحتوى الفلسفي والتأملي العميق هو ما يدعم استمرارية الأفكار الخاطئة والمفاهيم المربكة التي تعيق التعمق في فهم الكيمياء.
الفكرة الخامسة: المجموعة الثالثة
الفكرة الخامسة في هذه السلسلة من المقالات ستكون حول المجموعة الثالثة في الجدول الدوري:-
والتي تتكون من عناصر (ٍSc, Y, La, Ac) والآن أرى أنه يوجد دليل كافِ للقول بخطأ هذا الوضع للمجموعة.
ولكن في عام 1982 نشرت مجلة الــ “كيميكال إديوكيشن” مقال طُرِحت فيه فكرة ملخصها التالي:-
- أن المجموعة الثالثة يجب أن تظهر على النحو التالي: (Sc, Y, Lu, Lr).
وعلى الرغم من أنه تمّ الأخذ بهذا الوضع في بعض الكتب الأكاديمية إلا أنّ الكثير منها بدا رافضًا له [2].
الترتيبات السابقة فيما يخص المجموعة الثالثة
- كاتب المقال المنشور في عام 1982 لم يكن هو أول من رتّب المجموعة الثالثة على هذا النحو فالعديد من الجداول الدورية السابقة أظهرت نفس الترتيب،
- ولكن خمسينات وستينات القرن العشرين اقترح الفيزيائيون أن وضع عنصر اللوتيشيوم في المجموعة الثالثة أفضل من وضعه في آخر الصف الأول لعناصر الكتلة [f [3.
- ذكر الكاتب في مقاله المنشور عام 1982:-
أنّ الخطأ في تحديد البنية الإلكترونية لعنصر الإتيربيوم Yb ، قاد إلى وضع عنصر اللانثانوم La أسفل عنصر الإيتريوم Y في المجموعة الثالثة بدلا من عنصر اللوتيشيوم Lu، حيث افتُرضت البنية الإلكترونية لعنصري الإيتربيوم واللوتيشيوم كالتالي:
Yb: [Xe] 4f135d16s2
Lu: [Xe] 4f145d16s2
- وبناء على هذه التوزيعات المفترضة، أعطى الإلكترون الإضافي في مدار ال 4f لعنصر اللوتيشيوم تلميحًا أن هذا العنصر يجب أن يظهر في آخر موضع من الصف الأول لعناصر الكتلة f.
- القياسات الطيفية أظهرت أن كلا العنصرين يمتلكان 14 إلكترونًا في مدار[4f [4 ، نستطيع القول بأن هذه الحجة كذلك تنطبق على عنصر الإيتربيوم.
- ولكن إذا احتل عنصر الإيتربيوم الموضع الأخير من الصف الأول لعناصر الكتلة f، فسيحتل العنصر اللاحق له وهو عنصر اللوتيشيوم الموضع الأول من الصف الثالث للعناصر الانتقالية.
- ومنبدئيًا حسب البنية الإلكترونية لــ اللانثانوم، واللوتيشيوم يكون ممكناً لكليهم احتلال الموضع الثالث من الصف الأول لمجموعة العناصر الانتقالية.
(La: [Xe] 5d16s2 , Lu: [Xe] 4f145d1 6s2)
إذا احتل عنصر اللوتيشيوم لهذا الموضع تماشيًا مع ما يقترحه هذا المقال سيأخذ عنصر اللانثانوم الموضع الأول من عناصر الكتلة f. ولكن يوجد بعض الاعتراضات على هذا الترتيب وبسبب أن عنصر اللانثانوم لا يملك إلكترونات في مدار الـ f. ولكن هذا لا يعتبر شذوذ طارئ على الجدول الدوري مع عنصر اللانثانوم، وبسبب وجود العديد من الحالات التي تمّ تجاوز هذا الإلزام فيها فمثلًا عنصر الثوريوم Th لا يمتلك إلكترونات في مدار الـ f ومع هذا لا يوجد لدينا شك أنه ينتمي لعناصر الكتلة f.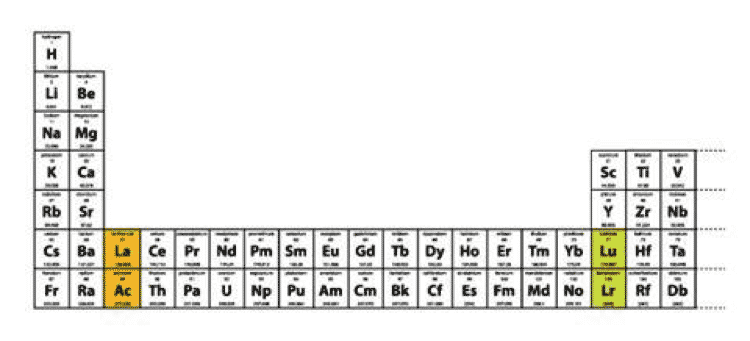 صورة 1جدول دوري ذو نمط طويل تظهر فيه العناصر مرتبة حسب ازدياد أعدادها الذرية
صورة 1جدول دوري ذو نمط طويل تظهر فيه العناصر مرتبة حسب ازدياد أعدادها الذرية
البنية الإلكترونية المفترضة هي في نهاية المطاف تقريبية لأقرب وصف يطابق البنية الواقعية. لذا الفرق بمقدار إلكترون واحد ليس هو نوع الاختلاف الذي يقرر ارتباط ذرة العنصر بأحد أجزاء الجدول الدوري. فذرات الهيليوم تمتلك إلكترونين في مدار الـ S وفي أغلب الترتيبات يوضع الهيليوم مع عناصر الكتلة [P [5.
الجداول الدورية ذات النمط الطويل
يوجد سبب آخر لتفضيل وضع عنصري اللوتيشيوم Lu واللورنسيوم Lr في المجموعة الثالثة بدلًا من عنصري اللانثانوم والأكتينيوم [6].
إذا وضعنا في اعتبارنا الجدول الدوري ذا النمط الطويل وأدخلنا عنصري اللوتيشيوم واللورنسيوم أو اللانثانوم والأكتينيوم في المجموعة الثالثة فإن الوضع الأول فقط هو الذي يكون مقبولًا يتسبب في تتابع مستمر في زيادة الأعداد الذرية (انظر إلى الصورة 1).
ولو وضعنا عنصري اللانثانوم والأكتينيوم في المجموعة الثالثة من الجدول الدوري ذي النمط الطويل سنحصل بسبب هذا الوضع حالتان من الشذوذ الواضح في تتابع الزيادة في الأعداد الذرية (انظر إلى الصورة 2).
صورة 2 – جدول دوري ذو نمط طويل فيه عنصري اللانثانوم والأكتينيوم في المجموعة الثالثة، ولكن في هذا الترتيب يفقد الجدول التتابع المستمر في زيادة الأعداد الذرية، وذلك لأن عنصر اللانثانوم عدده الذري 57 يظهر بين عنصرين لهم الأعداد الذرية 71و 72 وعنصر الأكتينيوم وله العدد الذري 89 يظهر بين عنصرين لهم الأعداد الذرية 103 و 104 .
الاحتمال الثالث
ولذلك بالنسبة لي فإن الجدل محسوم في تفضيل وضع عنصري اللوتيشيوم واللورنسيوم أسفل عنصري السكانديوم والإيتريوم في المجموعة الثالثة.
وفي الواقع يوجد احتمال لترتيب ثالث ولكن هذا الترتيب ينتج عنه انقسام غير متكافئ لعناصر الكتلة d (انظر الشكل 3)، وبسبب هذا التقسيم الغير موفق لعناصر الكتلة d، يكون هذا الترتيب أبعد التراتيب عن تمثيل الترتيب الصحيح للعناصر وأضعف من أن يمثل احتجاجًا على الوضع المقترح في هذا المقال للمجموعة الثالثة.
صورة 3 الخيار الثالث لإظهار الجدول الدوري ذي النمط الطويل وفيه تنقسم الكتلة d إلى جزأين غير متكافئين من مجموعة واحدة وتسع مجموعات.
ورد مؤخراً مقال في مجلة الــ “نيتشر” ونُشر في “البوبيلار ساينس” كمساهمة في الوصول إلى حل لمشكلة ترتيب المجموعة الثالثة [7] .
وللأسف على الرغم من أن أعضاء الفريق استخدموا نفس المعلومات والحقائق إلى أنهم توصلوا إلى نتائج مختلفة.
وهذا يؤكد على الحاجة الملحة لحل حاسم لهذه الإشكالية وأعتقد أن هذا ما قدمته في مقالي المنشور في الـ ” كمستري انترناشونال” [8].
ولكن على أي حال أقول أنه حان الوقت لهجر فكرة إظهار المجموعة الثالثة بالترتيب المتضمن على عناصر الــ Sc, Y, La , Ac.
الكاتب هو إيريك شيري مؤلف ومحاضر كيميائي في جامعة كاليفورنيا، لوس أنجلوس.
المصادر
- W B Jensen, Chem. Educ., 1982, 59, 634 (DOI: 10.1021/ed059p634)
- D W Oxtoby, H P Gillis and A Campion, Principles of Modern Chemistry, Brooks/Cole, 7th edn, 2012, p. 71. However, on the inside cover, the table shows lanthanum and actinium in group 3.
- L Landau and E M Lifshitz, Quantum mechanics, Pergamon, 1959, p. 245; D C Hamilton and M A Jensen, Rev. Lett., 1963, 11, 205 (DOI: 10.1103/PhysRevLett.11.205); D C Hamilton, Am. J. Phys., 1965, 33, 637 (DOI: 10.1119/1.1972042)
- Jensen implies that this reassignment of the configuration of ytterbium has been a ‘recent’ change. As a matter of fact, it was first made in 1937.
- This is not the case in the Janet or left-step periodic table, however, in which helium is placed in the s-block.
- E Scerri, A very short introduction to the periodic table, Oxford University Press, 2008, ch. 10
- T K Sato et al., Nature, 2015, 520, 209 (DOI: 1038/nature14342)
- The proposal was first made in E R Scerri, Int., July–August 2012, 34, 28
- Group Three, Education in chemistry. Retrieved November 12, 2017, from https://eic.rsc.org/opinion/five-ideas-in-chemical-education-that-must-die-part-five/2010032.article