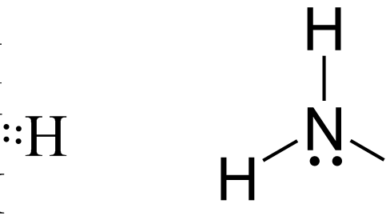
الخواص الفيزيائية والكيميائية لعنصر الليثيوم

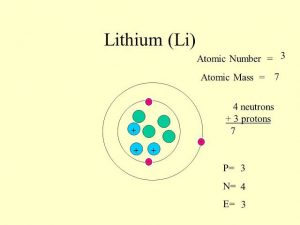
يُعد عنصر الليثيوم من العناصر الكيميائية، ويرمز له ب Li وعدد الليثيوم الذري 3، يوجد الليثيوم ضمن الجدول الدوري في عناصر الدورة الثانية وداخل المجموعة الأولى وهو أول الفلزّات القلويّة، أما الليثيوم النقي pure Lithium، فهو فلزّ لونه أبيض مائل للفضّي، وهو عنصر خفيف ولين، حيث أنّه أقل في الكثافة بالمقارنة بباقي العناصر الكيميائية الصلبة، وهذا عند حدوث ظروف قاسية من درجات حرارة وضغط.
يمكنك الاطلاع أيضًا على: التحلل الانتقائي لعنصر الذهب من مصادر متعددة المعادن في المحاليل العضوية
اكتشاف الليثيوم وتسميته
اكتشف عنصر ال Lithium المكتشف يوهان أوغست أرفويدسون السويدي الجنسية. فقد اكتشف في سنة 1817، تواجد عنصر غير مألوف في بيتاليت، وبعد ذلك بفترة قصيرة وجده في سبودومين ولبيدوليت.
عندما قام يوهان بتحليل تلك الاكتشافات التي وجدها في السويد في جزيرة أوتو، قام أستاذ يوهان الأكاديمي جون جاكوب بيرزيليوس بإطلاق اسم “ليثون” على الاكتشاف ، وهو مشتق من اسم “حجر الليثوس” اليوناني، وهو يشير إلى أسماء اثنين من المعادن القلوية أخرى، والتي يطلق عليها الصوديوم والبوتاسيوم، وبذلك انتشر الليثيوم في الشكل اللاتيني.
الخواص الفيزيائية والكيميائية لعنصر الليثيوم
بعد أن تم اكتشاف lithum قاموا بدراسة مجموعة من خواصه الفيزيائية والكيميائية، ومن تلك الخواص الأساسية له:
- يُعد الوزن الذرّي 6.941
- ويتواجد في الحالة الصلبة.
- ويظهر هذا العنصر في صورة معدن لونه فضّي وأملس.
- له درجة حرارة الذوبان والتي تُقدّر ب 453.65 كالفن، 180.50 درجة مئوية، أيضًا يحتوي على درجة الغليان والتي تتمثل في 1603 كالفن، 1330 درجة مئوية، 2426 فهرنهايت.
- تُقدّر الكثافة بمقدار 0.534 جرام/ سنتيمتر مكعب.
- له نقطة الانكسار: 67 نيوتن/متر مربع، درجة الانصهار: 3.00 كيلو جول/مول، درجة التبخر: 136 كيلو جول/مول.
- ويحدث تفاعل لليثيوم مع الماء والهواء والهالوجينات، كما بالأسفل.
يمكنك الاطلاع أيضًا على: حفّازات كيميائية بكلفة منخفضة تعزز استخلاص الهيدروجين من الماء
تفاعل عنصر Li مع الهواء
يتم قطع معدن Li بسهولة بسكين، سيظهر بسطح فضي لامع، ولكن هذا سرعان ما يتلاشى بسبب التفاعل مع الأكسجين والرطوبة من الهواء. عندما يتم حرق Li في الهواء ، فإن الناتج الرئيسي هو أكسيد الليثيوم الأبيض Li2O. يتم أيضًا إنتاج بعض بيروكسيد الليثيوم Li2O2، الأبيض أيضًا.
4Li (s) + O2 (g) → 2Li2O (s)
2Li (s) + O2 (g) → 2Li2O2 (s)
يتفاعل Li أيضًا مع النيتروجين N2 ، لتكوين نيتريد اللثيوم Li3N. لا يفعل أي من عناصر Gruop 1 الأخرى أي شيء مشابه ، لكن المغنيسيوم (Gruop 2) يشكل بالمثل نيتريدًا.
6 Li (s) + N2 (g) → 2Li3N
تفاعل الليثيوم مع الماء
تتفاعل معادن Li ببطء مع الماء من أجل تكوين محلول عديم اللون من هيدروكسيد اللثيوم (LiOH) وغاز الهيدروجين (H2). المحلول الناتج أساسي بسبب الهيدروكسيد المذاب. يكون التفاعل طاردا للحرارة، لكن التفاعل أبطأ من تفاعل الصوديوم (أسفل Li مباشرة في الجدول الدوري).
2Li (s) + 2H2O → 2LiOH (aq) + H2 (g)
تفاعل Li مع الهالوجينات
يتفاعل معدن Li بقوة مع جميع الهالوجينات من أجل تكوين هاليدات اللثيوم. لذلك ، يتفاعل مع الفلور ، F2 ، الكلور ، Cl2 ، البروم ، I2 ، واليود ، I2 ، لتكوين فلوريد اللثيوم (I) ، LiF ، الليثيوم (I) على التوالي ، LiCl ، الليثيوم (I) بروميد ، LiBr ، و يوديد.
2Li (s) + I2 (g) → LiI (s)
الاستخدامات والتواجد في الطبيعة
- الليثيوم يدخل بشكل أساسي في تصنيع السيراميك والزجاج
لأنه يتمتع بقدرة عالية في مقاومة درجات الحرارة المرتفعة، وبسبب احتياجه إلى درجات حرارة عالية حتى يحصل له تخريب، لذلك تدخل أكاسيد الليثيوم في صناعات الزجاج، حتى تتحسن مواصفاته وخصائص.
كما تعد “كربونات الليثيوم” (Li2Co3) عنصر رئيسي في تصنيع السيراميك؛ لأنه قادر على تقليل المعاملات الحرارية، وبذلك يحسن الخصائص الخاصة بالسيراميك المرتبطة بالحرارة.
- استخدامات الليثيوم في مجال الكهرباء والإلكترونيات
في آخر القرن العشرين، بات Li من العناصر الهامة في صناعة البطاريات إلى جانب الخلايا الكهربائية؛ وهذا يرجع إلى القدرة المرتفعة على التأين (أن تتحول لشوارد موجبة أو سالبة)، وبسبب أن كتلة الليثيوم الذرية قليلة، فله حرية بشكل كبير في المجال الخاص بالشحنات الكهربائية.
ومن أفضل ما يميز بطاريات Li أنها توفر أفضل أداء بالمقارنة بباقي البطاريات، حث تقوم بتوليد ما يقرب من 3 فولت لكل خلية بالمقارنة مع 2.1 فولت بالبطاريات المصنوعة من الرصاص و 1.5 بالبطاريات المصنوعة من الزنك والكربون.
- تخلص من بقع الزيت الموجودة على ملابسك
يعاني معظم الأشخاص من تواجد بقع زيت على ملابسهم، ويواجهون مشكلات متعددة لكي يخلصون منها، ولكن لقد وجد حل يسير للقضاء على تلك البقع. يعد Li من القواعد القويةوالتي تستخدم في تصنيع الصابون. وعندما يتم تسخينها مع نوع معين من الدهون ينتج عنها صابون، فتعاد صياغة مادة معينة تسمى “صابون الليثيوم”، يمتاز ذلك الصابون بأنه قادر على إزالة الزيوت بكل يسر.
المراجع
- Adityanjee, Munshi, Thampy, A, 2005, Neurotoxic disorder with irreversible lithium effect, Clen, 8, 38-49.
- Amdisen, 1978, Clinical examination and serum level in the treatment of lithium and lithium sugar, Centering, Toxicol, 2, 193–202.
- Baselt, R, 2008, Mien of Harmful Drugs and Chemicals in Man, 8th ed, Biomedical Distributions, City , Cultivation, California, 32, 56-67