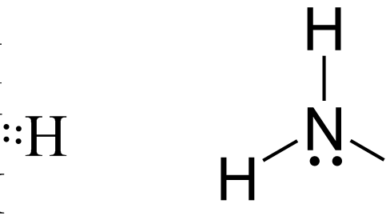
الخواص الكيميائية والفيزيائية لعنصر النيتروجين
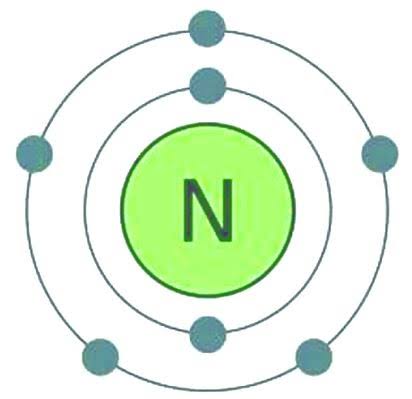
يشكل عنصر النيتروجين الجزء الأكبر من الغلاف الجوي للأرض78.1٪ من حيث الحجم، إنه ينتمي للمجموعة الخامسة عشر وهو على رأسهم وتسمي مجموعته بمجموعة النيتروجين، والدورة الثانية في الجدول الدوري. إنه غاز خامل جدًا عند درجة الحرارة والضغط القياسيين، لدرجة أنه أطلق عليه “azote” (بمعنى “بدون حياة”) في طريقة أنطوان لافوازييه للتسمية الكيميائية -ومع ذلك- فإن N جزء حيوي من إنتاج الغذاء والأسمدة ومكون من الحمض النووي لجميع الكائنات الحية.
يمكنك الاطلاع أيضًا على: حفّازات كيميائية بكلفة منخفضة تعزز استخلاص الهيدروجين من الماء
اكتشاف وتسمية عنصر النيتروجين
- أُخذت كلمة نيتروجين من الكلمة اللاتينية nitrum، واليونانية Nitron.
- اكتشف الكيميائي والطبيب (دانيال راذرفورد) النيتروجين في عام 1772.
حيث أزال الأكسجين وثاني أكسيد الكربون من الهواء، وأظهر أن الغاز المتبقي لن يدعم الاحتراق أو الكائنات الحية.
- في نفس العام تمكن كلًا من سكيل وكافنديش وبريستلي وآخرين من الحصول عليه.
- (ولكن وأطلقوا عليه “الهواء المحترق” أو “الهواء النفاث” الذي يعني الهواء بدون أكسجين).
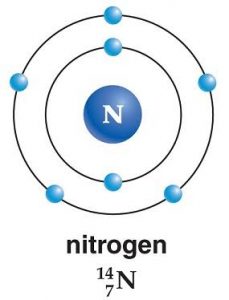
الخواص الفيزيائية والكيميائية لغاز النيتروجين
- غاز النيتروجين (الرمز الكيميائي N) خامل بشكل عام، يتواجد في الحالة الغازية.
- عنصر عديم اللون، وعديم الرائحة والطعم، وعدده الذري 7 ووزنه الذري 14.0067.
- تبلغ كثافة N2 1.251 جرام / لتر عند 0 درجة مئوية وكثافته النوعية 0.96737 ، مما يجعله أخف قليلاً من الهواء.
- عند درجة حرارة -210.0 درجة مئوية (63 كلفن) وبتركيز 12.6 كيلو باسكال، يصل N2 إلى نقطته الثلاثية (النقطة التي يمكن أن يتواجد عنصر فيها في الأشكال الغازية والسائلة والصلبة في وقت واحد).
وتشتمل الخواص الفيزيائية والكيميائية أيضًا على:
- عند درجات حرارة أقل من نقطة غليان N2 البالغة -195.79 درجة مئوية (77 كلفن)، يتكثف النيتروجين الغازي في نيتروجين سائل، وهو سائل يشبه الماء ويظل عديم الرائحة وعديم اللون، ولكن يتجمد N عند نقطة انصهار تبلغ- 210 درجة مئوية (63 كلفن) في مادة صلبة ناعمة تشبه الثلج.
- يوجد N في جميع الأنظمة الحية كجزء من تكوين المركبات البيولوجية.
- يمكن الحصول على غاز N2 عن طريق الإسالة والتقطير التجزيئي.
- يمكن أيضًا تحضير غاز N2 عن طريق تسخين محلول مائي من نتريت الأمونيوم (NH4NO3).
- يتصرف N2 كيميائيًا مثل اللافلزات، ويشكل النيتروجين مركبات في تسع حالات أكسدة مختلفة.
- لا يشكل النيتروجين مركبات كاتينية ثابتة بسبب التنافر بين أزواج وحيدة من الإلكترونات على الذرات المجاورة، ولكن يشكل روابط متعددة مع ذرات الفترة الثانية الأخرى.
- يتفاعل النيتروجين مع العناصر الموجبة للكهرباء لإنتاج مواد صلبة تتراوح من التساهمية إلى الأيونية.
- ينتج عن التفاعل مع الفلزات الكهربية الإيجابية نيتريد أيوني، والتفاعل مع معادن أقل حساسية للكهرباء ينتج نيتريدًا بينيًا، لكن التفاعل مع أشباه المعادن ينتج نيتريد تساهمية.
الترابط الجزيئي
يشكل N روابط ثلاثية التكافؤ في معظم المركبات.
يُظهر النيتروجين الجزيئي أقوى رابطة ثلاثية طبيعية ممكنة؛ بسبب الإلكترونات الخمسة الموجودة في الغلاف الخارجي للذرة.
تفسر هذه الرابطة الثلاثية القوية عدم نشاطها، إلى جانب القدرة الكهربية العالية للنيتروجين (3.04 على مقياس بولينج).
مركبات N في الطبيعة
- تتشكل نترات الصوديوم (NaNO3) ونترات البوتاسيوم (KNO3) عن طريق تحلل المواد العضوية مع وجود مركبات من هذه المعادن، توجد هذه الأملاح الصخرية بكميات كبيرة في بعض المناطق الجافة، والتي تستخدم كأسمدة.
- مركبات النيتروجين غير العضوية الأخرى هي حمض النيتريك (HNO3) والأمونيا (NH3) والأكاسيد (NO ، NO2 ، N2O4 ، N2O) ، السيانيد (CN-).
يمكنك الاطلاع أيضًا على: بثلاث طرق يمكن لدراسة الكيمياء العضوية تغيير دماغك!
استخدامات عنصر النيتروجين
- يعتبر غاز N2 مفيدًا في البيئات الصناعية والإنتاجية؛ بسبب وفرته وعدم نشاطه، ويدخل أيضًا في إنتاج الغذاء.
- يمكن لأنظمة إخماد غاز N2 أن تطفئ الحرائق دون خوف من التلوث.
- ويتم إنتاج الحديد والصلب والمكونات الإلكترونية الحساسة للأكسجين أو الرطوبة في جو من النيتروجين.
الأمونيا NH3
- يتفاعل الغاز الطبيعي (الميثان Methan) مع البخار لإنتاج ثاني أكسيد الكربون وغاز الهيدروجين (H2) في عملية من خطوتين.
- الأمونيا (NH3) هي أهم مركب تجاري للنيتروجين، يتم إنتاجه بواسطة عملية هابر، يتفاعل غاز الهيدروجين وغاز N2 عبر عملية هابر لإنتاج الأمونيا.
- هذا الغاز عديم اللون ذو الرائحة النفاذة، لذلك يسهل تسييله (في الواقع، يستخدم السائل كسماد نيتروجين).
- تستخدم الأمونيا أيضًا في إنتاج اليوريا NH2CONH2، الذي يستخدم كسماد.
- يستخدم في صناعة البلاستيك، ويستخدم أيضًا في صناعة الثروة الحيوانية كمكمل غذائي، غالبًا ما تكون الأمونيا هي المركب الأولي للعديد من المركبات النيتروجينية الأخرى
المراجع
- https://www.britannica.com/science/nitrogen/Properties-and-reaction
- Climates, Groffman, Dolah, Bernhardt, Grimm, NB, McMahon, 2016, Wildlife in Environmental Biology from a Community Perspective, The Longer Range is Boundless page 7-9
- Brady, and Weil, 2010, “Nutrient Cycles and Soil Fertility” in the Components of Soil Nature and Properties, 3rd edition, R Anthony (Upper Saddle River, NJ: Pearson Instruction Inc.), 396-420.