الجدول الدوري والخواص الدورية لعناصره

لمحة تاريخية عن الجدول الدوري:
خلال النصف الأول من القرن التاسع عشر، تم اكتشاف عدد كبير نسبياً من العناصر الجديدة، وتم التوصل إلى كثير من المعلومات المتعلقة بأوزانها الذرية، وخواصها الفيزيائية والكيميائية، ولهذا كان من الطبيعي أن تبدأ المحاولات الجدية لترتيب هذه المعطيات وتصنيفها ضمن ما عرف باسم الجدول الدوري للعناصر الكيميائية.
قام في عام 1829 دوبرينر Dobereiner بتوجيه الأنظار نحو وجود ثلاثيات في العناصر، بمعنى أن هناك مجموعات من العناصر، يتألف كل منها من ثلاثة عناصر متشابهة، يكون العنصر الأوسط منها ذي وزن ذري يساوي متوسط الوزن الذري للعنصرين الآخرين، وضرب منها مثلاً الثلاثية (I, Br, Cl) والثلاثية (Sr, Ba, Ca)، ثم تلت هذه المحاولة الجزئية في التصنيف محاولات عدة بغرض إيجاد علاقة بين خواص العناصر وأوزانها الذرية، ولكن أياً من هذه المحاولات لم يلق الصدى المناسب حتى عام 1860 بسبب عدم توفر أوزان ذرية للعناصر يمكننا الاعتماد عليها والاطمئنان لصحتها. وحتى ذلك الوقت الذي أيد فيه كانيزارو Cannizzaro صحة أفكار أفوكادرو Avogadro واستخدامها للحصول على الأوزان الذرية والأوزان الجزيئية عام 1859، وتوافق ذلك مع أعمال ستاس Stas الذي حدد بصورةٍ دقيقة بعض الأوزان الذرية للعناصر عام 1860.
ولعل من أكبر المحاولات التي جرت لتصنيف العناصر، محاولة أستاذ الكيمياء في جامعة لندن نيولاندز J. A. R. Newlands عام 1864 ترتيب العناصر المعروفة في حينه في مجموعات يتألف كل منها من ثمانية عناصر وفق ازدياد أعدادها الذرية، مُظهراً التشابه في الخواص الفيزيائية والكيميائية للعناصر في كل مجموعة، وهذا ما قاده إلى افتراض وجود قانون الثمانيات، ولكن اقتراحه جوبه بالسخرية لدى تقديمه إلى الجمعية الملكية، وبلغت السخرية حداً جعل أحد أعضاء الجمعية الملكية البارزين يقول: لو رتبنا العناصر وفق الأحرف الأبجدية لخرجنا بترتيب أفضل للعناصر من ترتيب نيولاندز.
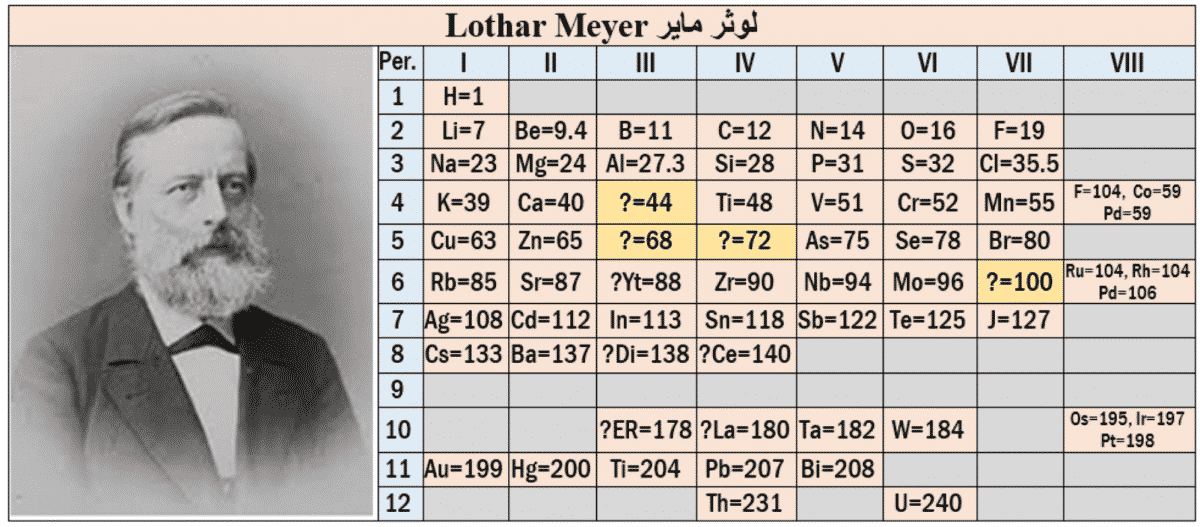
وأتت بعد أربع سنين محاولتان منفصلتان تماماً، ولكنهما متزامنتان تقريباً، حيث اقترح الألماني لوثر ماير Lothar Meyer عام 1860 عندما أعاد صياغة كتابه (النظريات الحديثة في الكيمياء) جدولاً دورياً يتألف من 56 عنصراً، وأظهر فيه علاقة بعض الخواص بالوزن الذري.
تصنيف الجدول الدوري لمندلييف:
وفي نفس الوقت تقريباً كان أستاذ الكيمياء في جامعة سانت بترسبرغ في روسية ديمتري مندلييف Mendeleyev يؤلف كتابه (مبادئ في الكيمياء)، واكتشف من خلال ترتيب هذا الكتاب مفتاح السر في ترتيب العناصر، وهكذا قدم ماندلييف نشرة في هذا الموضوع إلى الجمعية الكيميائية الروسية في اجتماعها عام 1869.
وفي عام 1882 مُنح ماندلييف وماير معاً جائزة ديفي، وهي أسمى جائزة تمنحها الجمعية الملكية البريطانية، وبعد مضي خمس سنوات على ذلك صحا ضمير هذه الجمعية فتذكرت محاولة نيولاندز وهو أحد أعضائها فمنحته نفس الجائزة تقديراً له وعرفاناً بفضله.
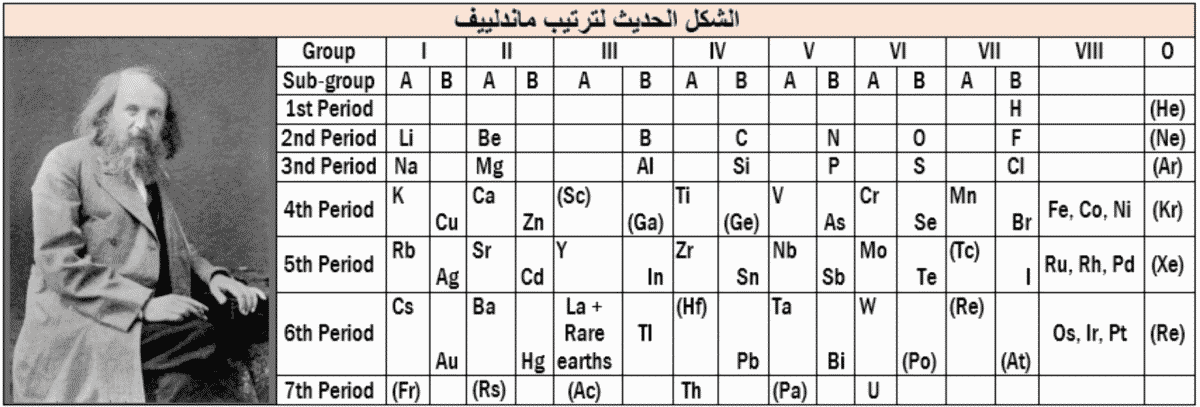
عرض ماندلييف ترتيبه للعناصر بطريقة تدل على الجرأة العلمية، والثقة العالية بالنفس، مما جعل تصنيفه الأساس الذي يبنى عليه أي ترتيب جديد للعناصر، وبدءاً من الهيدروجين فقد رتب ماندلييف العناصر المعروفة في وقته وفق ازدياد أعدادهها الذرية، وبيَّن وجود دورية في خواص العناصر، ولخص ذلك بالعبارة التالية: إن خواص العناصر توابع دورية لأعدادها الذرية، وللتأكيد على هذه العبارة رتب ماندلييف العناصر في جدول بحيث تقع العناصر المتشابهة تحت بعضها البعض، ويبين الجدول التالي شكلً حديثاً لترتيب ماندلييف للعناصر، ويتألف هذا الترتيب من سبعة صفوف أفقية تدعى الأدوار Periods، وتقع العناصر المتشابهة في الخواص تحت بعضها البعض، مشكلةً تسعة أعمدة من العناصر تدعى الفصائل Groups، ويتلاءم هذا الترتيب مع استخدام الأرقام العربية للدلالة على الأدوار، والأرقام الرومانية للدلالة على الفصائل.
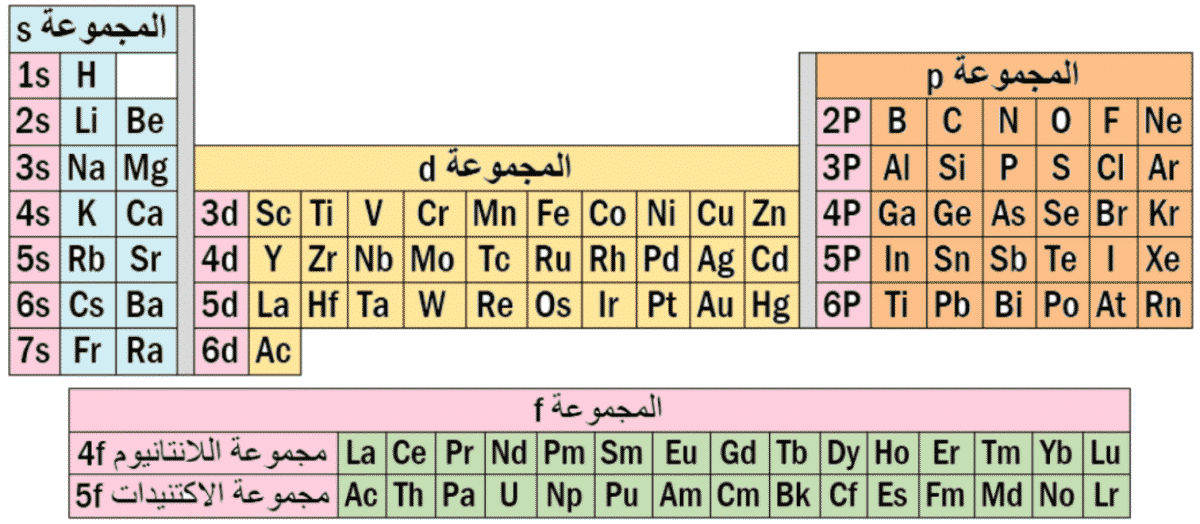
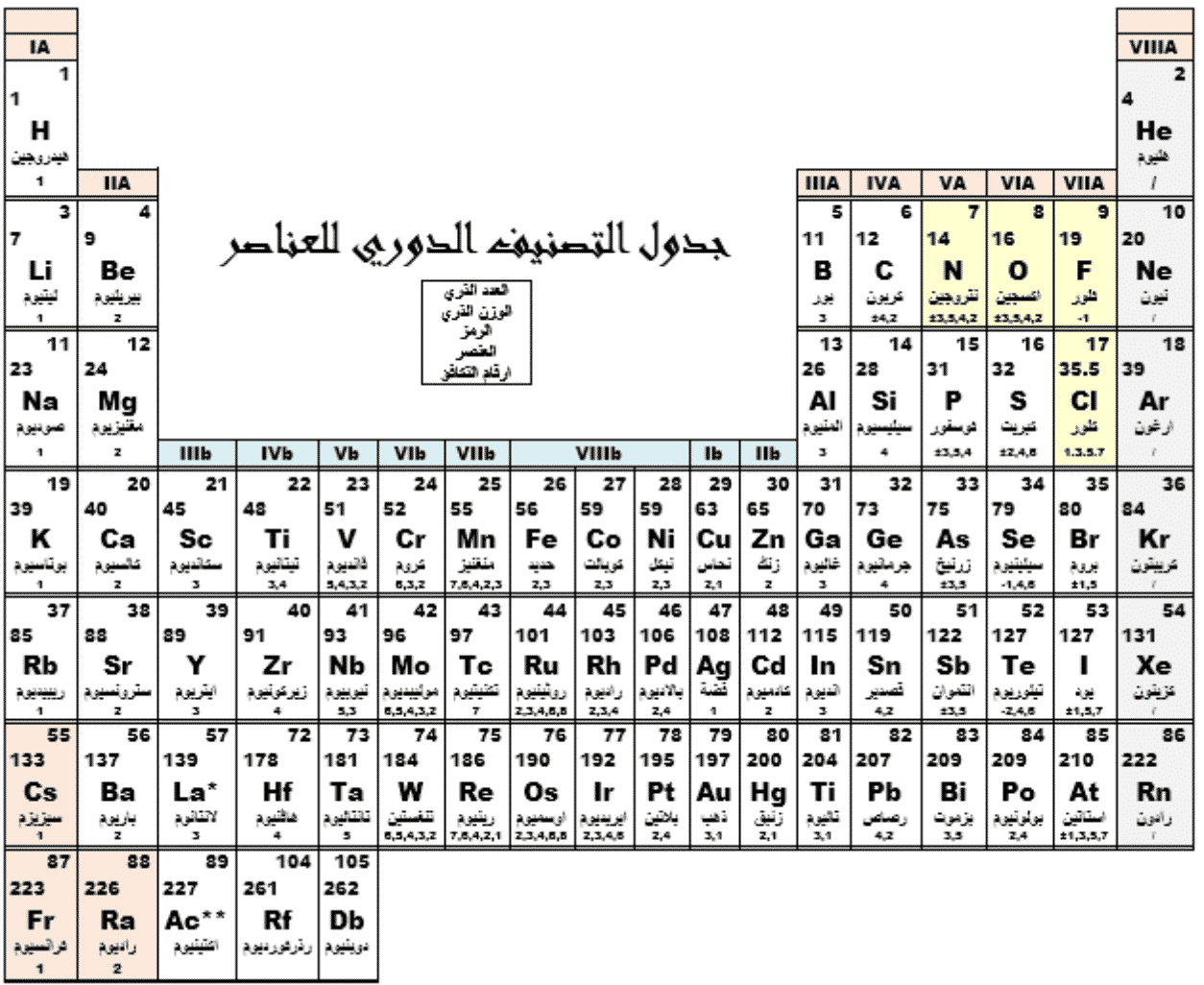 وتم اعتماد التصنيف التالي حديثاً:
وتم اعتماد التصنيف التالي حديثاً:
وتتغير الخواص الفيزيائية والكيميائية للعناصر دورياً تبعاَ لأعدادها الذرية، بسبب تغير بناها الالكترونية وفق نظامٍ محدد يجمع بينها، لذا سنتعرف أولاً على بعض مكونات وخواص الذرات لنتمكن من الولوج في عمق دراستنا في كيفية تغير هذه الخواص في الجدول الدوري وفقاً لتغير العدد الذري.
مكونات وخواص الذرات
1- أنصاف الأقطار الذرية (Atomic Radius):
يُقصد بالقطر الذري نصف المسافة الفاصلة بين نواتي ذرتين من ذرات العنصر في الجزيء الواحد، وتولي الدراسات الحديثة الأهمية الأكبر لنصف القطر الذري عن الحجم، لصعوبة تحديد الحجم الذري لعنصر بالدقة الكافية لتبدله مع تغيرات درجات الحرارة وشكل التركيب البلوري:
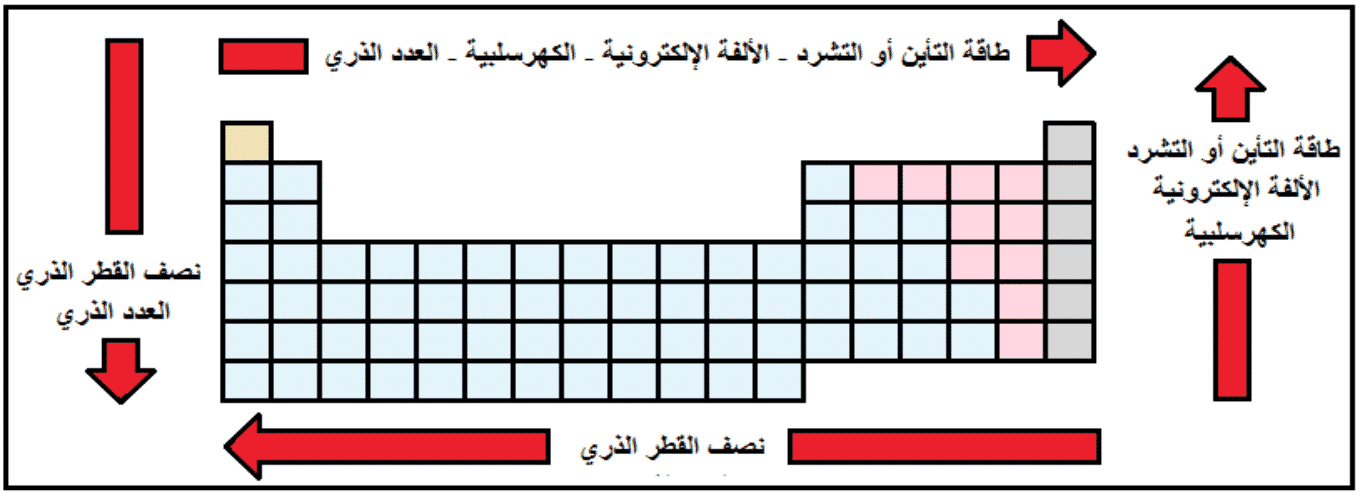
اتجاه تغير نصف القطر الذري عبر الدور والفصيلة في جدول التصنيف الدوري؟
في الدور الواحد: تتناقص الأقطار الذرية في الدور الواحد بازدياد العدد الذري، أي من اليسار لليمين، ويعود السبب في ذلك إلى تزايد الشجنة الفعالة لنوى ذرات العناصر في هذا الاتجاه، إذ تزداد شحنة النواة مع ازدياد محتواها من البروتونات الموجبة الشحنة، ما يزيد من قدرتها على جذب الكترونات الطبقة السطحية، فتتقلص هذه الطبقة ويتناقص بالتالي نصف القطر.
مثال: قارن بين أنصاف أقطار الذرات التالية: 3Li, 5B, 9F:
نلاحظ أن جميع هذه العناصر تقع في ذات الدور، وبالتالي فإن الكتروناتها تتوزع على الشكل:
3Li: 1s2, 2s1
5B: 1s2, 2s2, 2p1
9F: 1s2, 2s2, 2p5
وبالتالي يمكننا ترتيبها بحسب ازدياد نصف القطر الذري على اعتبار أن نصف القطر الذري يتناقص مع ازدياد شحنة النواة على الشكل:
F → B → Li
تزايد →
في الفصيلة الواحدة: تزداد أنصاف أقطار ذرات الفصيلة الواحدة مع ازدياد العدد الذري، أي من الأعلى للأسفل برغم تزايد شحنة النواة في ذات الاتجاه، ويعود السبب في ذلك لازدياد عدد الطبقات الالكترونية عند الانتقال من الأعلى للأسفل، وهو ما يطغى على ازدياد شحنة النواة.
2- طاقة التأين (Ionization energy):
تتميز العناصر المعدنية بقدرة ذراتها على التخلي عن الكتروناتها الخارجية لتتحول إلى أيونات موجبة الشحنة، لذا تُعرَّف طاقة التأين على أنها: (الطاقة المبذولة لانتزاع الكترون من ذرة معتدلة X منفردة وبحالتها الغازية).
Xg + energy+ → Xg + e–
يدل هذا التعريف على طاقة التأين الأولى (Ii)، أما في حال كانت الذرة متعددة الكترونات الطبقة السطحية فيمكننا الإشارة بذات الطريقة لكل طاقة تأين، فتكون طاقة التأين الثانية على الشكل:
Xg+1 + energy+ → Xg+2 + e–
تقدر طاقة التأين بالالكترون فولط لذرة واحدة، أو بواحدة الكيلو جول لجزيئة غرامية واحدة (أي لمول واحد): KJ.mol-1. ويتم قياس طاقة التأين للذرات في حالتها الغازية المفردة لتجنب تأثير الذرات المجاورة.
تغير طاقة التأين عبر الدور والفصيلة في جدول التصنيف الدوري؟
في الدور الواحد: تزداد طاقة التأين في الدور الواحد بازدياد العدد الذري، أي من اليسار لليمين، ويعود السبب في ذلك إلى تزايد الشحنة الفعالة لنوى ذرات العناصر في هذا الاتجاه، إذ تزداد شحنة النواة مع ازدياد محتواها من البروتونات الموجبة الشحنة، ما يزيد من قدرتها على جذب الكترونات الطبقة السطحية، وبذلك تزداد طاقة التأين.
في الفصيلة الواحدة: تتناقص طاقة تأين الفصيلة الواحدة مع ازدياد العدد الذري، أي من الأعلى للأسفل برغم تزايد شحنة النواة في ذات الاتجاه، ويعود السبب في ذلك لفعل الحجب الذي يلعبه ازدياد عدد الطبقات الالكترونية عن الالكترونات الخارجية عن النواة، وبالتالي تناقص تأثره بها فتقل طاقة التأين.
وتكون شحنة النواة المؤثرة في الكترونات التكافؤ أدنى من شحنتها الظاهرة كونها محجوبة عنها بالالكترونات الداخلية الأقرب إليها.
مثال: رتب العناصر التالية تصاعدياً بحسب ازدياد طاقة التأين: (4Be, 7N, 9F). نكتب الترتيب الالكتروني للعناصر، فنجد أن جميعها يقع في ذات الدور:
4Be: 1s2, 2s2
7N: 1s2, 2s2, 2p3
9F: 1s2, 2s2, 2p5
Be → N → F
تزايد →
3- الألفة الالكترونية (Electron affinity):
تميل ذرات بعض العناصر في الجدول الدوري لاستكمال طبقتها الالكترونية الخارجية وخاصة العناصر اللامعدنية منها لاكتساب الكترونات إضافية وبالتالي تشكيل أيونات سالبة، وهو ما يوصف بالألفة الالكترونية والتي يمكننا تعريفها على أنها: (الطاقة المتحررة عند ضم الكترون واحد إلى ذرةٍ غازية معتدلة لتشكيل أيون سالب في حالة مستقرة). وتقدر بالكيلو جول للمول الواحد (KJ.mol-1):
Xg + e– → Xg– + energy
وتلزمنا طاقة ثانية وثالثة لإضافة الكترونات إضافية إلى الأيون السالب للتغلب على قوى التنافر الكهربائية.
تغير الألفة الالكترونية عبر الدور والفصيلة في جدول التصنيف الدوري؟
في الدور الواحد: تزداد الألفة الالكترونية في الدور الواحد بازدياد العدد الذري، أي من اليسار لليمين، ويعود السبب في ذلك إلى تزايد الشحنة الفعالة لنوى ذرات العناصر في هذا الاتجاه، إذ تزداد شحنة النواة مع ازدياد محتواها من البروتونات الموجبة الشحنة، ما يزيد من قدرتها على جذب الكترونات الطبقة السطحية.
في الفصيلة الواحدة: تتناقص الألفة الالكترونية في الفصيلة الواحدة مع ازدياد العدد الذري، أي من الأعلى للأسفل برغم تزايد شحنة النواة في ذات الاتجاه، ويعود السبب لفعل الحجب الذي يلعبه ازدياد عدد الطبقات الالكترونية عن الالكترونات الخارجية عن النواة، والذي يؤدي لتنافرٍ بين الالكترونات السطحية والالكترون الجديد.
مثال: رتب العناصر التالية تصاعدياً حسب ازديد الألفة الالكترونية (19K, 32 Ge, 35Br). نكتب التوزيع الالكتروني لهذه العناصر، فنجد أنها جميعاً تنتمي لدورٍ واحدٍ:
19K: 1s2, 2s2, 2p6, 3s2, 3p6, 4s1
32Ge: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 4d10, 4p2
35Br: 1s2, 2s2, 2p6, 3s2, 3p6, 4s2, 4d10, 4p5
K → Ge → Br
تزايد →
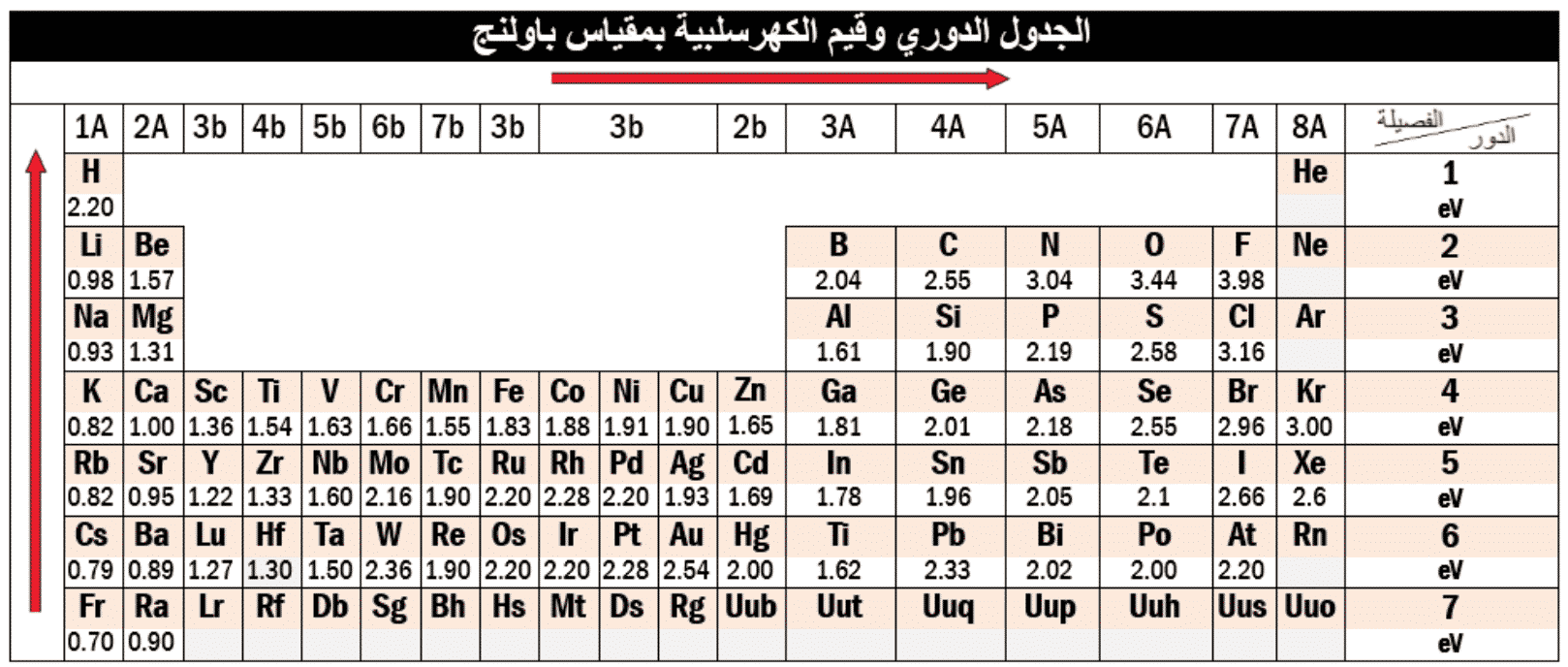
4- الكهرسلبية (Electronegativity):
تميل بعض عناصر الجدول الدوري لفقدان بعض الكتروناتها أثناء تفاعلاتها الكيميائية لتصير أيونات موجبة، في حين يميل بعضها الآخر لاكتساب الكترونات لتصير أيونات سالبة، وتسمى العناصر من النوع الأول وهي المعادن غالباً اسم العناصر الكهرجابية، في حين تسمى عناصر النوع الثاني وهي اللامعادن وأشباه المعادن العناصر الكهرسلبية.
تغير الكهرسلبية عبر الدور والفصيلة في جدول التصنيف الدوري؟
في الدور الواحد: تزداد الكهرسلبية في الدور الواحد بازدياد عدد الالكترونات السطحية، أي من اليسار لليمين.
في الفصيلة الواحدة: تتناقص الكهرسلبية في الفصيلة الواحدة ضمن الجدول الدوري مع ازدياد العدد الذري، أي من الأعلى للأسفل برغم تزايد شحنة النواة في ذات الاتجاه، ويعود السبب لفعل الحجب الذي تلعبه ازدياد عدد الطبقات الالكترونية عن الالكترونات الخارجية عن النواة، ما يؤدي لإضعاف قدرتها على جذب الالكترونات.
مثال: رتب العناصر التالية بحسب تزايد كهرسلبيتها (15P, 16S, 17Cl). نكتب التوزيع الالكتروني لها فنلاحظ أنها جميعا تقع في الدور الثالث:
15P: 1s2, 2s2, 2p6, 3s2, 3p3
16S: 1s2, 2s2, 2p6, 3s2, 3p4
17Cl: 1s2, 2s2, 2p6, 3s2, 3p5
P → S → Cl
تزايد →
ومن المفيد أن نذكر هنا أن العالم مليكان Millikan قد وضع قانوناً لقياس الكهرسلبية على أساس أنها متوسط طاقة التأين والألفة الالكترونية، أي أن:
EN = K[(I+EA)/2]
حيث: EN: الكهرسلبية، K: ثابت التناسب وقيمته (1/2.8)، I: طاقة التأين، EA: الألفة الالكترونية.
5- الكترونات التكافؤ (Valence electrons):
الكترونات التكافؤ هي الالكترونات الموجودة على الطبقة السطحية لأي عنصر. ويعرَّف تكافؤ أي عنصر على أنه عدد الالكترونات التي تفقدها أو تشارك بها الذرة عند تكوين مركب كيميائي، وتشغل هذه الالكترونات عادةً في ذراتها بحالتها المستقرة المدارات العالية السوية الطاقية.
- قيم تكافؤات عناصر الفصائل (IA: 1, IIA: 2, IIIA: 3, IVA: 4): عدد الكترونات التكافؤ في الذرات المعنية.
- قيم تكافؤات عناصر الفصائل (VIIIA: 1, VIIA: 2, VIA: 3, V): تساوي الفرق بين العدد الأعظمي (ثمانية الكترونات) وعدد الكترونات تكافؤها.
- ذرات العناصر النبيلة (الخاملة) والتي تشكل الفصيلة الثامنة VIIIA تملك ثمانية الكترونات تكافؤ، عدا ذرة الهليوم التي تحوي الكتروني تكافؤ فقط.
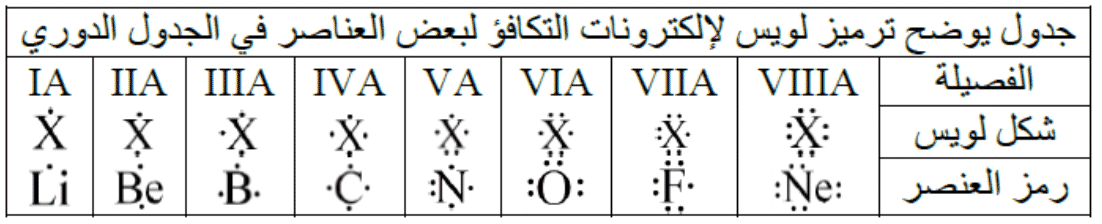
اعتمد العالم لويس ترميزاً لالكترونات التكافؤ كنقاط تحيط برمز العنصر تساوي في عددها رقم الفصيلة:
مثال: اكتب التركيب الالكتروني للعناصر الافتراضية التالية (X, Y, Z)، ما عدد الكترونات التكافؤ في كل عنصر؟ نكتب الترتيب الالكتروني لكل عنصر فنجد:
8X: 1s2, 2s2, 2p4 | عدد الكترونات التكافؤ=6
6Y: 1s2, 2s2, 2p2 | عدد الكترونات التكافؤ = 4
9Z: 1s2, 2s2, 2p5 | عدد الكترونات التكافؤ = 7
6- الخاصة المعدنية والخاصية اللامعدنية:
في الدور الواحد: تتناقص الخاصة المعدنية في الدور الواحد من يسار الجدول إلى يمينه بسبب تناقص أنصاف الأقطار الذرية (أنصاف الأقطار الذرية والأيونية)، وكمونات التأين أي سهولة إزاحة الالكترونات، فنجد أن الخاصة المعدنية تتناقص من الليثيوم مثلاً وصولاً حتى الفلور، ومن الصوديوم حتى الكلور، فلو قارنا أطوال أنصاف أقطار الدور الثاني لوجدناها على الشكل:
في الفصيلة الواحدة: تزداد الخاصة المعدنية في الفصيلة الواحدة ضمن الجدول الدوري مع ازدياد نصف القطر الذري، أي من الأعلى للأسفل. فلو قارنا أطوال أنصاف أقطار الفصيلة الأولى (IA) لوجدناها على الشكل:
يؤدي تزايد أنصاف أقطار العناصر في الدور الواحد من اليمين إلى اليسار للتخلي عن الكتروناتها بسهولةٍ أكبر، لذا نجد أن ذرات العناصر المعدنية كبيرة، بينما تكون ذرات العناصر اللامعدنية صغيرة. كما نجد أن المعادن التي تتصف بخواص معدنية نموذجية هي المعادن القلوية مثل الصوديوم، وأكثرها قلوية هو الفرانسيوم الذي يتمتع بخواص إرجاعية عالية.
أما ذرات العناصر اللامعدنية فتميل لضم الالكترونات لتصبح بنيتها الالكترونية شبيهة ببنية الغاز النادر المستقرة، وعليه فإن تشكل أيون سالب في ذرة لها نصف قطر صغير أسهل بكثير من تشكل هذا الأيون في ذرةٍ أكبر قطراً. فاللامعادن النموذجية (باستثناء العناصر النادرة) هي فصيلة الهالوجينات، وأكثرها صفةً معدنية هو الفلور.
وأخيراً نجد أن أكثر العناصر المشكلة للحموض هي العناصر الواقعة أعلى الجدول الدوري، والعناصر المشكلة للأسس هي العناصر الواقعة أسفله، فهيدروكسيد الفوسفور حمضية التفاعل، أما هيدروكسيد البزموت فأساسي التفاعل.