تقدير أيون الكلوريد في الماء

يعد أيون الكلوريد من الأيونات السالبة المهمة الموجودة في المياه الطبيعية ويكسب الماء الطعم المالح إذا ارتبط مع أيون الصوديوم مكوناً كلوريد الصوديوم (ملح الطعام) تتصف أملاح الكلوريدات بقابليتها العالية على الذوبان في الماء. إنّ وجود أيون الكلوريد بتركيز عالٍ في الماء له تاثير سام في المزروعات وتحتوي فضلات المياه المنزلية والصناعية نسبة عالية من الكلوريد، وقد صنفت مياه الري حسب محتواها من الكلوريد الى أربعة اصناف كما في الجدول أدناه:
| صنف الماء | تركيز الكلوريدملي مكافئ/لتر | مدى ملائمة الماء |
| (1) قليل | أقل من 2 | الماء صالح للنباتات جميعها تقريباً |
| (2) معتدل | 2-4 | الماء صالح للنباتات المتحملة للكلور مع ظهور أضرار طفيفة الى متوسط على النباتات الحساسة للكلور |
| (3) متوسط | 4-8 | الماء صالح للنباتات جيدة التحمل للكلور مع ظهور أضرار طفيفة الى متوسط على النباتات الأقل تحملاً للكلور |
| (4) شديد | أكثر من 8 | الماء لايزال يصلح للنباتات جيدة التحمل للكلور التي يمكن أن تظهر عليها أضرار طفيفة الى متوسط |
طريقة مور Mohr’s Method
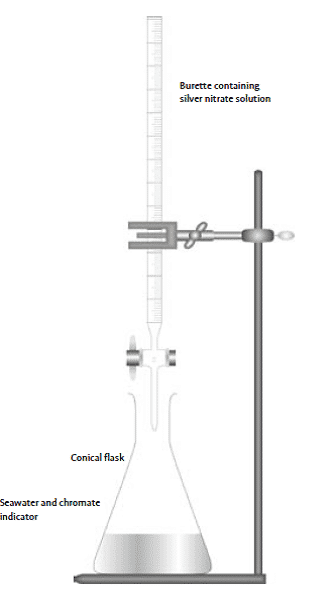 تعد طريقة التسحيح (طريقة مور) الطريقة المعتمدة لتقدير أيون الكلوريد في المياه الملوثة من قبل جمعية الصحة الامريكية والهندية والهولندية. حيث تتم بتسحيح 100 مل من عينة الماء مقابل محلول نترات الفضة (0.014 عياري) وباستخدام كاشف كرومات البوتاسيوم لغاية تغير اللون للعينة (البني الفاتح) ويعبر عن النتائج بملغرام كلورايد لتر بعد أخذ معدل قرائتين.
تعد طريقة التسحيح (طريقة مور) الطريقة المعتمدة لتقدير أيون الكلوريد في المياه الملوثة من قبل جمعية الصحة الامريكية والهندية والهولندية. حيث تتم بتسحيح 100 مل من عينة الماء مقابل محلول نترات الفضة (0.014 عياري) وباستخدام كاشف كرومات البوتاسيوم لغاية تغير اللون للعينة (البني الفاتح) ويعبر عن النتائج بملغرام كلورايد لتر بعد أخذ معدل قرائتين.
المحاليل المستخدمة:
1. محلول دليل كرومات البوتاسيوم K2CrO4:
يحضر من إذابة (50gm) من كرومات البوتاسيوم K2CrO4 في كمية قليلة من الماء المقطر ثم يضاف إلى المحلول قطرات من محلول نترات الفضة AgNO3 إلى أن يتكون راسب أحمراً واضحاً. يترك المحلول لمدة24 ساعة ثم يرشح للتخلص من الراسب ويخفف الراشح إلى لتر بالماء المقطر.
2. محلول نترات الفضة القياسية (0.0141N):
يحضر من إذابة 2.395 غرام من نترات الفضة في قليل من الماء المقطر ثم يكمل الحجم إلى لتر بالماء المقطر ويحفظ هذا المحلول في قناني زجاجية غامقة اللون brown bottle
3. محلول كلوريد الصوديوم (0.0141N)
يجفف مسحوق كلوريد الصوديوم بدرجة حرارة (140) درجة مئوية ولمدة ساعتين، بعدها يبرد ويوزن بدقة 0.8241gm من المسحوق المجفف، يذوب بالماء المقطر في قنينة حجميه سعة واحد لتر.

Ag+(aq) + Cl–(aq) → AgCl(s)
2Ag+(aq) + CrO42-(aq) → Ag2CrO4(s)
تدابير العمل (Procedure):
- يؤخذ 100.0 مل من الماء المقطر ويستخدم مقارناً Blank.
- يكمل 10.0 مل من ماء العينة إلى 100.0 بالماء المقطر.
- يضاف 1.0 مل من محلول ثنائي كرومات البوتاسيوم ككاشف إذ يلاحظ ظهور اللون الأصفر.
-

بعد التسحيح يسحح كل من المحلول المقارن والعينة مع محلول نترات الفضة (0.0141N) لحين ظهور اللون القهوائي.
- يسجل حجم نترات الفضة ويعاد ثلاث مرات.
يعبر عن النتائج بوحدات ملغم .لتر-1 باستخدام المعادلة الآتية:
حجم العينة/ mg Cl–/L = (A-B) x N x 35450
حيث:
A = حجم نترات الفضة النازل من السحاحة لتسحيح العينة.
B = حجم نترات الفضة النازل من السحاحة لتسحيح المقارن.
N = عيارية نترات الفضة (0.0141N (AgNO3
ملاحظة: M.eq of NaCl = 35.450
ويجب أن تكون pH للماء بمدى 6.5-9. حيث يمكن إزالة شوارد الفضة عند قيمة pH مرتفعة بترسيبها مع شوارد الهيدروكسيد، وعند قيم pH منخفضة يمكن إزالة شوارد الكرومات بواسطة تفاعل حمض-أساس لتشكيل شوارد الكرومات الحامضية أو شوارد ثنائي الكرومات.
المصدر:
APHA (American public Helth Association). (2005). Standard methods for examination of water and wastewater, 21th Ed. Washington DC, USA.

جميل جدا.. حبذا لو يتبعها مقالات مشابهة عن بقية الطرق المعروفة، مثل طريقة فاجان وفولهارد ،والطرق المعتمدة على المطيافية الضوئية!!