ما هي الكحولات أو الأغوال
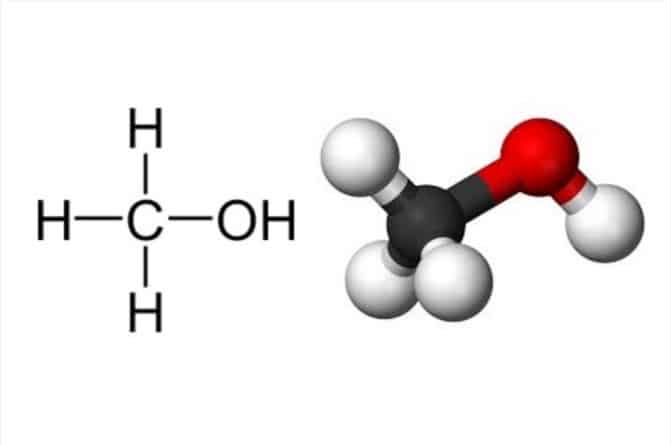
إن الكحولات أو الغولات هي عبارة عن مجموعة المركبات العضوية التي تحمل مجموعة هيدروكسيل (OH) واحدة على الأقل، وتتحد مع مجموعة ألكيل، ومن المعروف أن الإيثانول أو ما يعرف باسم الكحول الإيثيلي هو العنصر الأساسي، والرئيسي في جميع الكحوليات التي يتناولها البعض، وفي موضوع اليوم، سوف نتناول الكحولات والخواص الفيزيائية والكيمائية لها، وسنتعرف أيضًا على طرق التحضير وسنعرف كيف تصنف الكحوليات وما السبب في التسمية بذلك، والأن هيا بنا في جولة قصيرة في عالم الكحولات.¹
يمكنك الاطلاع أيضًا على: حفّازات كيميائية بكلفة منخفضة تعزز استخلاص الهيدروجين من الماء
الخواص الفيزيائية والكيميائية للكحولات
الكحولات موجودة بشكل كير حولنا، ولكن لها خواص فيزيائية وكيميائية، تميزها عن غيرها، وهي كالتالي:
- مجموعة الهيدروكسيل الموجودة بالمركبات العضوية تزيد من قطبيتها، ومن ذوبانها في الماء.
- غالبًا لا يكون لها لون وتكون شفافة.
- كلما زاد عدد ذرات الكربون في المركبات الكحولية عن 12 ذرة، كلما ذادت درجة صلابة الكحول في درجة الحرارة العادية.
- درجة غليان الكحول أعلى من درجة غليان المركبات الهيدروكربونية الأخرى، والألكانات، ولكن كلما زاد عدد ذرات الكربون كلما ارتفعت درجة الغليان.²
- يمكن اعتبارها قواعد وأحماض ضعيفة.
- تعتبر الكحولات مشتق عضوي من الماء، الذي تتم فيه تبديل ذرتي الهيدروجين بمجموعة من الألكيل.
- الكحولات تدخل في العديد من الصناعات الحياتية مثل :-
كصناعة العطور، المعقمات الطبية، وصناعة الوقود، ولكن بنسب معينة من إضافة الكحول.³
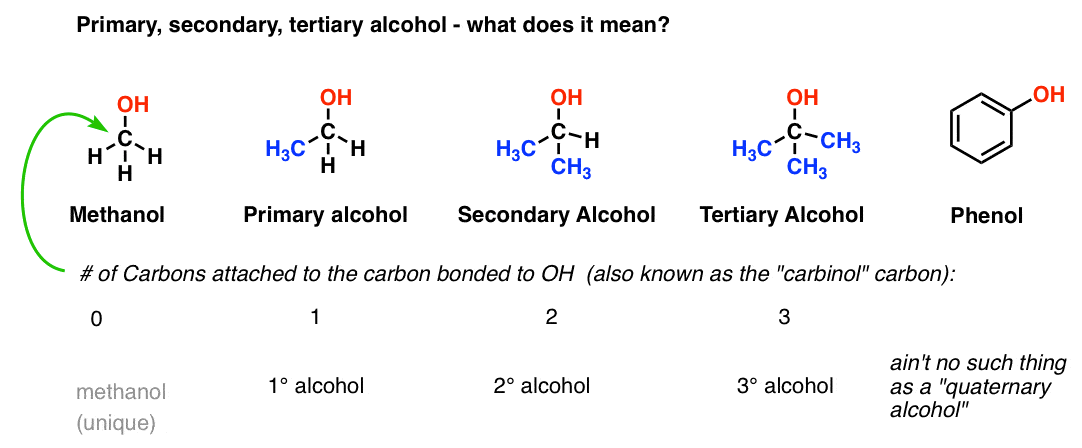
تصنيف الكحولات
تصنف الكحولات إلى أربعة أقسام، ولكن ذلك تبعًا لعدد مجموعة الهيدروكسيل بها، ويتم التصنيف بالشكل التالي ذكره.
أحادية الهيدروكسيل
وهي تلك الكحولات التي تمتلك مجموعة هيدروكسيل واحدة، مثل الكحول الإيثيلي أو ما يعرف بالإيثانول.
ETHANOL ورمزه الكيميائي C2H5OH، والصيغة الجزئية له C2H6O .
ثنائية الهيدروكسيل
وهي تلك التي تمتلك مجموعتين من الهيدروكسيل، مثل الإيثيلين جلايكول Ethylene glycol.
رمزه الكيميائي C2H6O2، والصيغة الجزئية له C₂H₄(OH)₂.
ثلاثية الهيدروكسيل
وهي تلك التي تمتلك ثلاث مجموعات من الهيدروكسيل مثل الجليسرول أو ما نعرفه باسم الجلسرين ورمزه الكيميائي C3H8O3. ⁴
متعددة الهيدروكسيل
وهي تلك التي تمتلك أكثر من ثلاث مجموعات من الهيدروكسيل مثل السوربيتول Sorbitol، ورمزه الكيميائي C6H14O6.

كيف تتم التسمية
يتم إطلاق الأسماء على الكحولات بطريقتين وهما كالآتي:
- عن طريق (IUPAC) وهو ما يعرف بالإتحاد الدولي للكيمياء البحتة والتطبيقية.
وهذا بحذف أخر حرف موجود في مجموعة الألكان واستبداله بحرفي (OL) مثل:-
METHANE→ METHANOL، تم تحول الميثان إلى ميثانول.
Glycerol → Glycerin، تم تحويل الجليسرين إلى جليسرول.
- عن طريق استخدام الأشم الشائع.
- ويتم هذا عن طريق إضافة “الكيل” مثل الإيثانول Ethanol يطلق عليه كحول الإيثيل Ethyl Alcohol.⁵
يمكنك الاطلاع أيضًا على: Applied Chemistry كيمياء تطبيقية
كيف يتم تحضيرها
يمكن تحضير الكحولات بعدة طرق أهمها ما يأتي:-
اختزال الكربون
- ويتم عن طريق إضافة ذرتين من الهيدروجين إلى الكربوكسيلك أسيد، أو إلى الكيتون أو ألداهيد.
- وتكون بإضافة الهيدروجين أو أي عامل مختزل أخر.
هدرجة الألكينات
وتكون بإضافة الهيدروجين إلى مجموعة الألكين التي بها رابطة ثنائية، ونتيجة لذلك نحصل على الكحول.
إزاحة الهاليدات
يتم في هذا التفاعل استبدال لمجموعة الهاليد بالهيدروكسيل، ونتيجة لذلك نحصل على الكحول. ⁴
- C12H22O11 → C6H12O6 + C6H12O6
- Invertase → glucose + fructose
- C6H12O6 + H2O → C2H5OH + CO2
- Glucose → zymase + ethanol
- ***
- [CO + H2] + H2O (g) → CH3OH
- ***
-
- 2 R-OH + 2 NaH → 2 R-O–Na+ + H2↑
- 2 R-OH + 2Na → 2R-O−Na+
- مثلا 2 CH3CH2-OH + 2 Na → 2 CH3-CH2-O−Na+
وبهذا نكون أنهينا موضوعنا اليوم، ونأمل أن نكون استطعنا تقديم الإفادة الكافية لكم عن الكحولات وطرق تحضيرها وتصنيفها، وأن تكونوا عرفتم أيضًا ما هي الخواص الفيزيائية والكيميائية للكحولات وكيف يتم تسميتها.
المراجع
- Morrison R and Boyed R., “Organic Chemistry”, Allyn and Bacon, Unused York, 1987.
- Brewster R, “Organic Chemistry”, Prentice-Hall, London 1958.
- Zaczek N, ” Sodium Borohydride as a Lessening Specialist for Aldehydes And Ketones”, Vol, 63,No of 5,PP.909-919, 1986.
- Farrar W,” Diphenyl Diselenide Amalgamation by Gringnard Official AND Selenium Metal”, Investigated (London), Vol. 4, PP, 177-215, 1951.