نوبل العرب وتفاعلات الفيمتو ثانية

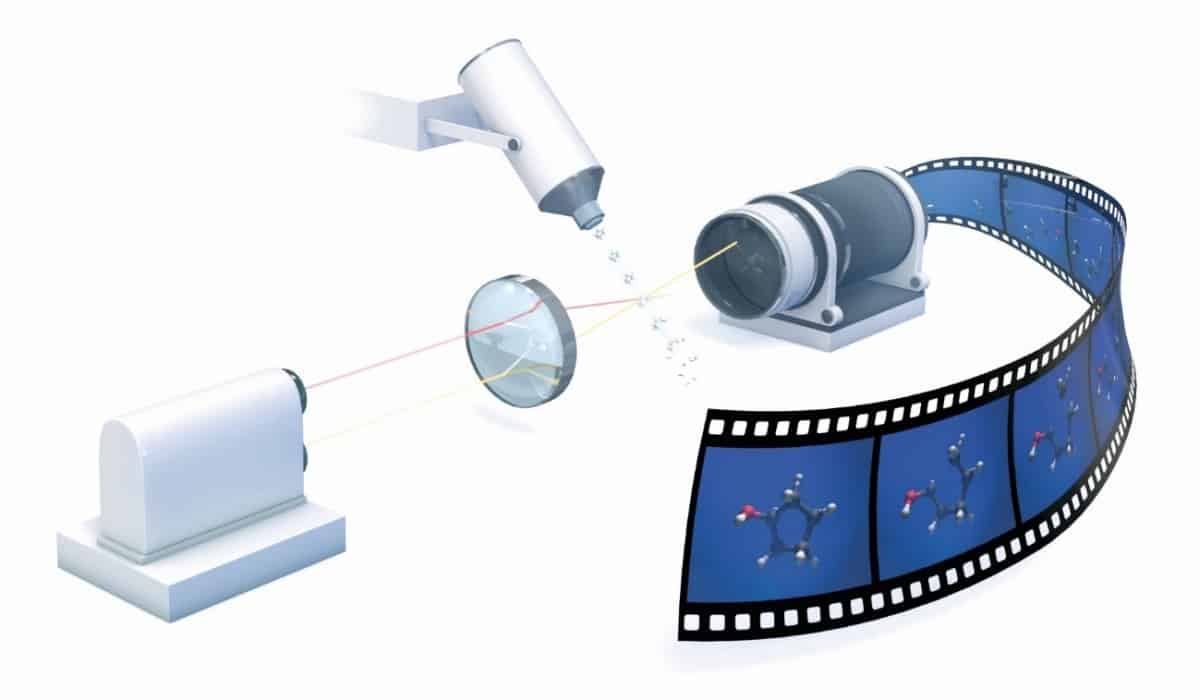
عندما تدخل الجزيئات ضمن التفاعلات الكيميائية، تتحرك ذراتها بسرعة بحيث لا يمكن مشاهدتها. لكن تخيل فيما لو استطعنا تصوير العملية باستخدام كاميرا عالية السرعة، ويمكنها إعادة إظهار التفاعل بحركة بطيئة. دفع فضول الكيميائيين لتطوير طرق متقدمة من شأنها دراسة أدق تفاصيل التفاعل الكيميائي. وكانت النتائج حصول العالم المصري أحمد زويل على جائزة نوبل عام 1999 وذلك لأبحاثه في مجال جديد من الكيمياء … “كيمياء الفمتو”. سنلقي من خلال هذا المقال على سبب حصول البروفسور زويل على هذه الجائزة، وما هي حقيقة وأهمية كيمياء الفمتو في عملية البحث العلمي.
استخدم البروفسور أحمد زويل طريقة، يمكن وصفها بأنها أسرع كاميرا حتى الآن. تتم باستخدام ومضات ليزرية، يكون الزمن بين الومضات منخفض جداً بحيث يمكننا النزول لمستويات زمنية صغيرة والتي تقارب سرعة التفاعلات الكيميائية، أي الفمتوثانية Femtosecond. الفمتوثانية هو 10-15 من الثانية، أي ما يقابل ثانية واحدة لـ 32 مليون سنة! يسمى مجال الكيمياء الفيزيائية الذي نشأ على هذه الدراسات بكيمياء الفمتو Femtochemistry.
سمحت لنا كيمياء الفمتو بفهم الآليات التي تسمح بحدوث بعض التفاعلات، بينما لا تحدث التفاعلات الأخرى، ولماذا تكون سرعة التفاعل والمردود تابعان لدرجة الحرارة. على ضوء أبحاث البروفسور أحمد زويل، استطاع العلماء حول العالم دراسة التفاعلات باستخدام مطيافية الفمتوثانية Femtosecond Spectroscopy في الغازات، السوائل، الأجسام الصلبة، السطوح، على البوليميرات والنظم البيولوجية. يشمل مجال التطبيقات بدءاً من كيفية عمل الحفازات وكيف يمكن تصميم الجزيئات في الأجهزة الالكترونية، حتى التفاعلات الحيوية.
-
سرعة التفاعلات الكيميائية:
من المعروف أن التفاعلات الكيميائية تحدث بسرعات كبيرة، وعادةً ما تزداد سرعة التفاعل مع ارتفاع درجة الحرارة، لتصبح حركة الجزيئات أكثر عنفاً ويزداد احتمال اصطدام الجزيئات.
وضعت أول معادلة لربط التفاعلات الكيميائية بدرجة الحرارة من قبل الكيميائي السويدي سفانت أرينيوس Svante Arrhenius (حصل على جائزة نوبل سنة 1903)، وذلك سنة 1889:
حيث k هي ثابت سرعة التفاعل، A ثابت، Ea طاقة التنشيط، k في الأس هو ثابت بولتزمان، T درجة الحرارة المطلقة.
تعبر طاقة التنشيط عن ارتفاع الحاجز الطاقي اللازم تجاوزه لحصول التفاعل الكيميائي، والذي تصل عنده الجزيئة لحالة طاقية عالية، وقد أسماه أرينيوس بالمعقد المنشط Activated Complex.
تم تطوير معادلة أرينيوس على يد هنري أيرينغ Henry Eyring ومايكل بولاني Michael Polanyi وذلك بطرح نظرية الحالة الانتقالية Transition State Theory، والتي تم اشتقاقها من حركية المواد على المستوى الجهري.
-
ولادة مجال بحثي جديد
لقد استخدم الضوء العادي لكشف التفاعلات الكيميائية: كل جزيئة تملك لوناً مختلفاً عن الأخرى، لذلك يتم استخدام جهاز المطيافية الضوئية Spectrophotometer لتعقب تحولات (حركية) المتفاعلات إلى النواتج، وكانت البدايات الاولى في تطوير طرق لتبطيىء التفاعلات الكيميائية حتى أزمنة قصيرة من مرتبة الميلي ثانية.
استطاع الكيميائيين بالطرق القديمة اكتشاف وجود المركبات الوسطية Intermediates وهي مركبات تقع في حالة بين المواد المتفاعلة والمواد الناتجة، ولا تعد هذه المركبات ضمن سلم الثواني مستقرةً. إن كل مساهمة في تحسين دقة الزمن اللازم لكشف المركبات الوسطية، قد قاد إلى دراسة عمر المركب الوسطي ضمن أزمنة قصيرة جداً والتي يكون عندها هذا المركب، بشكل تقريبي: مستقراً.
أما اليوم، وبفضل تقدم مجال كيمياء الليزر والتي تعتبر أساس أبحاث البروفسور زويل، فيمكن تعقب التفاعلات الكيميائية بدقة تصل حتى بليون مرة بجعل حزم الجزيئات تتصادم بالفراغ وباستخدام ومضات ليزرية فرق الزمن بين الومضتين منخفض جداً.
مع نهاية ثمانينيات القرن الماضي، قام زويل بسلسلة من التجارب والتي أدت لولادة مجال بحثي جديد والذي يسمى اليوم بكيمياء الفمتو. يمكن وصفه أنه باستخدام أسرع كاميرا يمكنها التقاط صور للجزيئات أثناء تفاعلها خصوصاً عند مرحلة الحالة الانتقالية. طبعاً الكاميرا عبارة تقانة ليزرية متقدمة، تصدر ومضات بفارق زمني من مرتبة الفمتوثانية.
إنّ مساهمة أحمد زويل هي إمكانية الوصول لأقصر أزمنة تفاعل ممكنة، لا يوجد تفاعلات كيميائية تحدث أسرع منها. ينتقل الحديث من حركية التفاعل إلى ديناميكية التفاعل. باستخدام مطيافية الفمتوثانية، يمكننا ولأول مرة، مراقبة مرحلة عبور الحاجز الطاقي بشكل كما لو أننا نشاهد فيلماً أبطأ مما هو عليه، وبالتالي يمكننا من فهم الخلفية الميكانيكية لمعادلة أرينيوس.
-
تجربة أحمد زويل
قام أحمد زويل، من أجل الحصول على “الفيلم الجزيئي” لتفاعل كيميائي، بمزج المتفاعلات على شكل حزم جزيئية ضمن غرفة مخلاة من الهواء. كما هو العادة في مرحلة التفاعل أحادي الجزيئة، يكفي لحدوث التفاعل نوع واحد من الحزم الجزيئية. قام بعد ذلك بتشغيل ليزر عال السرعة، حيث يكون الزمن بين نبضتين ليزرتين عدة مئات من الفمتوثانية، وذلك لضخ نبضتين على الجزيئة الواحدة: الاولى هي نبضة ضخ عالية الطاقة والتي تقوم بإثارة الجزيئة لحالة طاقية عالية والتي يبدأ عندها التفاعل. تأتي بعدها نبضة ليزرية أضعف من الاولى، تسمى بنبضة المئبر، تختار طول الموجة من أجل لكشف الجزيئة الأصلية أو الشكل البديل عنها.
بدأت تجارب أحمد زويل الاولى على تفاعلات التفكك أحادية الجزيئة لسيانيد الصوديوم إلى جذور اليود والسيانيد:
ICN → I + CN
وقد نشر فريقه البحثي مقالة في مجلة فيزياء الكيمياء Chemical Physics سنة 1987، تتحدث عن دراسة الحالات الانتقالية ضمن مجال الفمتوثانية، حيث تمت مراقبة تكسير الرابطة الكيميائية I-C والتي تمت خلال 200 فمتوثانية.
قام فريق أحمد زويل سنة 1988 بدراسة تفارق dissociation يوديد الصوديوم:
NaI → Na++I–
حيث أثارت النبضات الليزرية الزوج الأيوني Na+I– والذي كان له مسافة توازنية بين النوى تساوي 2.8A0، لتتحول إلى الشكل المثار [fusion_builder_container hundred_percent=”yes” overflow=”visible”][fusion_builder_row][fusion_builder_column type=”1_1″ background_position=”left top” background_color=”” border_size=”” border_color=”” border_style=”solid” spacing=”yes” background_image=”” background_repeat=”no-repeat” padding=”” margin_top=”0px” margin_bottom=”0px” class=”” id=”” animation_type=”” animation_speed=”0.3″ animation_direction=”left” hide_on_mobile=”no” center_content=”no” min_height=”none”][Na-I]* والذي كان له طول رابطة أقصر والتي تملك صفة الرابطة التكافؤية (مشتركة). على أية حال، فإن خواصها تتغير عندما تهتز الجزيئة: عندما تكون ذرات الصوديوم واليود عند مواضع تحولها الخارجي، 10-15 A0 بعيداً عن الالكترون، تكون البنية أيونية
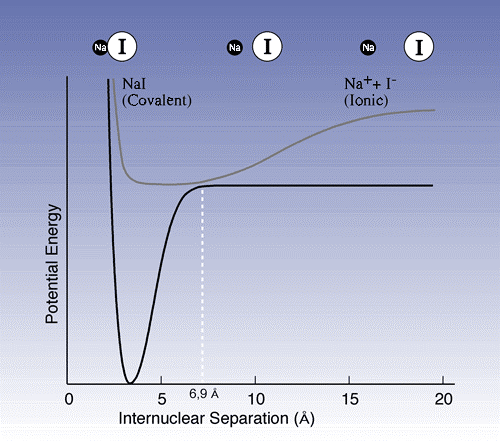
يتم الوصول لنقطة حرجة أثناء الاهتزاز وذلك عند مسافة 6.9A0، وهي عندما عندما تكون الحالة المثارة، والحالة الأساسية قريبتان جداً من بعضهما. عند هذه النقطة يكون هناك احتمال كبير بأن الحالة المثارة [Na-I]* سوف تعود لحالتها البدائية [Na-I]، أو تتفكك لذرات الصوديوم واليود. يمثل الشكل 1منحنيات الطاقة الكامنة، حيث يمثل المنحني العلوي الحالة المثارة، والمنحني السفلي هو الحالة البدائية.
ما وجده زويل وفريقه أنه يمكن تتبع المعقد المنشط عندما يتحرك إلى الأمام والخلف، أي بين الرابطة التكافؤية والرابطة الأيونية.
تم تفسير ذلك بأن النبضات الليزرية قد شكلت عينة من الجزيئات المثارة تبدأ جميعها عند النقطة 2.8A0 وتهتز بعدها بشكل متزامن. ثم سوف تمر جميع الجزيئات عند النقطة السحرية 6.9A0 بنفس الوقت، مما يفسر لماذا تفاعلت الجزيئات كلها بنفس الوقت تقريباً وبالتالي التشكيل الاهتزازي لذرات الصوديوم.
أحد التفاعلات التي تمت دراستها هو تفاعل تماكب الستيلبين Stilbene بوجود مصدر ضوئي، كما يظهر في الشكل 2:
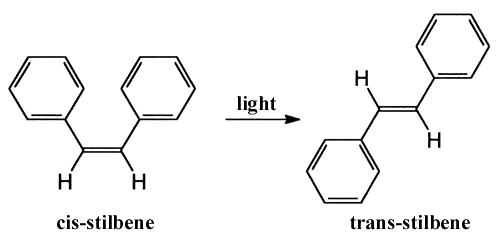
خلال إثارة الشكل المقرون للستيلبين cis-Stilbene باستخدام نبضة فمتوثانية، سوف تضعف الرابطة الثنائية المركزية الشبيهة بالإيتيلين، مما يسمح بدوران حلقات البنزن بزاوية 900 إلى مركب وسطي ملتوي خلال 300 فمتوثانية، مما يعطي في النهاية الشكل المفروق trans-Stilbene بزاوية دوران 1800. تمت ملاحظة هذه الظاهرة من قبل باحثين آخرين على مركب الريتينال retinal، وهو جزء من صبغة الرودوبسين rhodopsin المسؤولة عن التقاط الضوء في عين الانسان. يمكن تفسير الفعالية العالية للتفاعل (70%) من خلال معدل التفاعل الكبير (200 فمتوثانية) واكتشاف الاهتزاز المترابط والذي يستمر إلى الاهتزاز في المركب النهائي.
المصدر:
Autobiography Ahmed Zewail. (n.d.). The Nobel Prize in Chemistry. Retrieved October 11, 2015, from http://zewail.nobel-link.com/1.htm
Femtochemistry. (n.d.). Physical Biology Center for Ultrafast Science & Technology (UST) – Caltech. Retrieved October 11, 2015, from http://www.ust.caltech.edu/press/femtochem.html
The 1999 Nobel Prize in Chemistry – Extended version of the Press release. (n.d.). Nobel Prize. Retrieved October 11, 2015, from http://www.nobelprize.org/nobel_prizes/chemistry/laureates/1999/advanced-chemistryprize1999.pdf
[/fusion_builder_column][/fusion_builder_row][/fusion_builder_container]