المول وثابت أفوجادرو: رحلة مفهوم كيميائي من 1811-2018

ثابت أفوجادرو في حياتنا اليومية، من المعتاد أن نستخدم عدة طرق لقياس الأشياء؛ فنستخدم الغرام أو الكيلو غرام للكتلة، واللتر أو متر مكعب للحجم. ونستخدم مثلاً كلمة “زوج pair” أو كلمة “دزينة أو درزن dozen” للإشارة لعدد معين من الشيء فالزوج للدلالة على عدد 2، و الدرزن للدلالة على عدد 12. بغض النظر عن نوعية الشيء المعدود، وقياس الشيء بالعدد سنُركز عليه لوضوح البقية و لتداخل هذا نوع من القياسات مع موضوع المول.
نقول:
- زوج إطارات أي 2 من الإطارات، زوج جوارب أي 2 من الجوارب ، درزن أكواب أي 12 كوب …الخ
وهنا عدة ملاحظات على قياس الشيء بالعدد:
- هذه الكلمات غير مرتبطة بشيء محدد، فنستخدمها للإطارات أو الجوراب أو غيرهما على حد سواء.
- من الواضح أنّ كتلة الإطارات تختلف عن كتلة الجوارب مع أنّ عددهما متساوي، وكتعميم أنّ تساوي القياس بالعدد لشيئين لا يعني بالضرورة تساوي القياسات الأخرى لهذين الشيئين.
- تُستخدم هذه الكلمات للأشياء العيانية (الماكروسكوبية macroscopic) والتي يُمكن أن تُرى بالعين.
إلا أنّ ما يتعامل معه الكيميائيون في مختبراتهم هي أشياء (ذرات أو جزيئات) مجهرية (مايكروسوبية microscopic)، فما هي الطريقة المناسبة للتعامل معها؟
في البداية تم استخدام مقياس الوزن الذري والذي يختصر بـ (atomic weight (amu or u or Da من قبل جون دالتون صاحب النظرية الذرية وهي قيم بدون وحدات. وهذه القيم تُقاس نسبة لعنصر الهيدروجين الذي أخذ قيمة “وحدة واحدة” فيما بعد استخدموا عنصر الأوكسجين بسبب قابليته الكبيرة للإتحاد مع العناصر المختلفة وبالتالي سهولة تحديد الوزن الذري للعناصر نسبة لعنصر الأوكسجين الذي أخذ قيمة 8. وأيضًا أُستخدم الكيميائيون الوزن المكافيء Equivalent Weight.
وفي نهاية القرن التاسع عشر تقريباً طُرح مفهوم “المول mole” الذي يدلُّ الآن (حسب تعريف 1971) على عدد معين للأشياء الموجود في كتلةٍ محددة من أحد العناصر، والتي اُعتبرت هذه الكتلة مِقياس (معيار) لبقية الكتل. وسُمّي هذا العدد المعين من الأشياء بـ عدد أفوجادرو (أو ثابت أفوجادرو) تكريمًا للعالم الإيطالي أميدو أفوجادرو باعتباره صاحب الفكرة الأساسية النظرية لتحديد العدد، وقد مرّ مفهوم المول بعدة مراحل حتى عصرنا الحاضر (بدايات القرن الحادي والعشرين)
و هذا المقال ملخص لتأريخ هذا المفهوم:
1811 والولادة الضبابية
بعد أن اصطدمت نظرية دالتون الذرية مع قانون غي لوساك التجريبي بخصوص التفاعلات الحجمية. تقدم أميدو أفوجادرو عام 1811 بمفهوم الجزيئة مع فرض علمي وملخصه:
“إنّ الحجوم المتساوية من الغازات المختلفة تحتوي على العدد نفسه من الجزيئات، إذا كانت الظروف (ضغط + حرارة) متشابهة، وبغض النظر عن طبيعة هذه الغازات أو نوعها.”
هذا الحدس العلمي لأفوجادرو ربط بين عدد الجزيئات والحجم، وعُرف هذا الحجم فيما بعد، بالحجم المولاري القياسي للغاز ويُساوي 22.41 لتر تقريباً.
إلا أنّ مفهوم الجزيئة بقي شبه مهمل لمدة 50 سنة تقريبًا بعد هذه الفرضية العلمية، باستثناء بعض العلماء الذين أيدوا مفهومه وحدسه.
بينما كان من الرافضين لمفهوم الجزيئة دالتون نفسه صاحب النظرية الذرية “باعتبار أنّ ذرات العنصر الواحد لا يُمكن أن تتجاذب مع بعضها البعض”. وقد أجابت نظرية الكوانتم عن ذلك فيما بعد.
1826 محاولة تطبيقية لحدس أفوجادرو
نشر الكيميائي الفرنسي دوما Jean-Baptiste Dumas في هذا العام طريقة لتحديد الكُتل الذرية عن طريق معرفة كثافة بخار المواد (سواء كانت سائلة أو حتى صلبة) بالاعتماد على فرضية أفوجادرو.
1860 المؤتمر الدولي الأول للكيميائيين لحدس أفوجادرو
بعدما توفي أفوجادرو بسنوات قليلة عُقد المؤتمر الدولي الأول للكيميائيين 1860 في ألمانيا، حيث أعاد العالم الإيطالي كانزيرو الحياة لمفهوم الجزيئة والفرض العلمي الذي تقدم به أفوجادرو من خلال إمكانية تحديد الكتل الذرية والجزيئية النسبية للمركبات والعناصر بواسطة فرض أفوجادرو.
1865 التحديد الأول لعدد الجزيئات

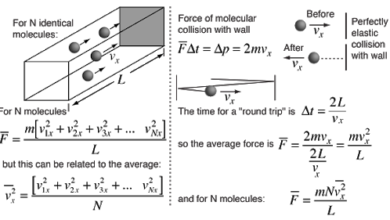
قام جوزيف لوشميدت Loshmidt Joseph في ورقة بحثية نشرها. وبالاعتماد على حسابات ماكسويل وكلاسيوس، بمحاولة لحساب عدد الجزيئات في 1 سنتيمتر مكعب تحت الظروف القياسية STP في موضوع النظرية الحركية للغازات. وكان العدد الذي توصل إليه 8.66 × 1710 جزيئة في السنتيمتر المكعب.
وفي هذه السنة تقريباً، استخدم الكيميائي الألماني هوفمان August Wilhelm Hofmann لأول مرة في الكيمياء مصطلحي الـ مولر Molar (والتي كانت في الأصل تُشير الى أي كتلة كبيرة) Macroscopic و Molecule (والتي تُشير إلى كتلة صغيرة أي microscopic)، ومع هذا فمصطلح المولر تم استخدامه بعد ذلك (وبشكل مقيد) لكتلة المادة بالغرام الذي يعكس كتلة مكوناتها بوحدة الكتلة الذرية.
1873 إعادة حساب العدد

استخدم ماكسويل J. Maxwell النظرية الحركية في انتشار الغاز وحصل على عدد لوشميدت (السابق) وكان مقداره 1.9 × 1910.
1894 ولادة المفهوم
في هذا العام (وبعض المصادر تُشير بأنه عام 1892 أو 1893 أو 1896) أطلق الكيميائي الألماني أوستوالد Ostwald مصطلح “مول mole” أول مرة للإشارة إلى وزن غرامات المادة الذي يُماثل عددياً الوزن الجزيئي للمركب أو الوزن الذري للعنصر. بعبارة أخرى استخدم المفهوم للإشارة إلى كتلة كبيرة big mass بعكس مفهوم molecule الذي يشير إلى الكتلة الصغيرة small mass.
وأغلب المصادر تُشير إلى أنّ كلمة mole مشتقة من اللغة اللاتينية moles وتعني “كومة” أو “كدس” أو “تجمّع كُتل صغيرة”. وهناك من يفترض أنّ

المصطلح أتى من الألمانية، و هو اختصار لكلمة Molekülargewicht و (Molekül) تعني جزيء.
من الطريف في الموضوع، أنّ فيلهلم أوستوالد عند طرح المفهوم كان يُهاجم فيه النظرية الذرية-الجزيئية. ومحاولته تقديم بديل عن ذلك للحساب الكيميائي Stoichiometry. ومن المعروف أنّ النظرية الذرية أخذت وقت كثير حتى تم قبولها في الأوساط العلمية.
على أية حال، قد يُطرح تساؤل: الغرام هو وحدة كتلة المادة، لكن المول وحدة ماذا؟ أوستوالد لم يقل شيئاً عن ذلك.
1897 ترجمة المفهوم إلى اللغات الأخرى
تمت ترجمة مصطلح مول (mol) من اللغة الألمانية إلى اللغة الإنجليزية (mole) كما في كتاب The Principles of Mathematical Chemistry: The Energetics of Chemical Phenomena الصادر 1897، وتقول مصادر أخرى أنّ الاستخدام الأول في اللغة الإنجليزية كان عام 1902.
1905 – 1906 الحركة البراونية ورؤية الذرات!
ألبرت أينشتاين A. Einstein في ورقته البحثية لأطروحة الدكتوراه “عن حجم الجزيئات” حاول أن يُبرر وجود ذرات ذات حجم محدود ومحدد، ونظريته زودت طريقة لحساب عدد الجزيئات من خلال ملاحظة تأثيرها الجماعي على جسيم أكبر مغمور، وأيضًا قام باشتقاق معادلات لمعاملات الانتشار واللزوجة حيث يُستنتج منها عدد أفوجادرو، ومن القيم التجريبية لمعاملات الانتشار واللزوجة لمحلول السكر في الماء حصل على مقدار (لما سُمّي فيما بعد بعدد أفوجادرو) مساوٍ لـ 2.1 × 1023. وفي بحث آخر مستمد من عمله للدكتوراه تم تحسين البيانات التجريبية فحصل على مقدار لعدد أفوجادرو مساوٍ لـ 4.15 × 1023.
من جهة أخرى، وبالرغم من أنّ ظاهرة الحركة البراونية كانت مكتشفة أقدم من هذا التاريخ (اكتشفت 1828)، إلا أنّ في هذا التاريخ قام أينشتاين بتطبيق النظرية الحركية عليها وأعطى طريقة لتحديد عدد أفوجادرو من دون إعطاء قيمة معينة له!
1909 حساب عدد الجزيئات في غرام جزيئي
استخدم الفرنسي بيرين Jean Perrin مجهر فائق ultra-microscope أُخترع حديثاً –في وقته– للتأكد من صحة نظرية أينشتاين بخصوص الحركة البراونية. وأيضًا تقدم بفرضية “أي جزيئين غراميين سيحتويان دائمًا على العدد نفسه من الجزيئات، وهذا العدد ثابت كوني و م المناسب تمييزه باسم عدد أفوجادرو.
وكان العدد الذي توصّل إليه في بداية الأمر هو: 7.05 × 1023 وكتب بورقته البحثية هكذا 70.5 × 1022 لكن التجارب اللاحقة أكدت العدد بدقة 1 × 1023.
قدمت أعمال بيرين دليل مباشر على الطبيعة الذرية للمادة (تذرّي المادة أو انفكاكها)، ويُعد تقديره لعدد أفوجادرو أقدم تقدير تجريبي مقارب للقيمة المعمول بها حالياً. وكتوضيح لفرضيته بخصوص احتواء الجزيئات الغرامية على العدد نفسه:
من المتفق عليه –كيميائيًا– أنّ لكل ذرة عنصر كتلة نسبية تُقاس بعدة وحدات كالغرام أو وحدة الكتلة الذرية amu. في بعض أنواع التفاعلات الكيميائية (مثل تفاعلات التعادل) عند خلط أو تفاعل كتلتين مختلفتين من عنصرين أو مركبين مختلفين (بحيث كل كتلة تُساوي الكتلة النسبية الغرامية للمركب أو العنصر) فإنّ التفاعل ينتهي باختفاء هذه المواد المتفاعلة نهائيًا وتكوّن مادة جديدة، فماذا يعني ذلك؟
فلنقرأ الأمر بصيغة أخرى:
مواد ذات كتل مختلفة تفاعلت واختفت بتكوّن مادة جديدة، والتفاعل الكيميائي يحدث عند اتحاد ذرة مع ذرة أخرى (على الأقل) مما يعني أن هذه الكتل من المواد بالرغم من اختلاف كميات كتلتها، فإنّ جميع ذراتها قد اتحدت مع بعضها واختفت بتكوّن مادة (مركب) جديدة، ومما يُستنتج من هذا: أنّ عدد الذرات في هذه الكتل المختلفة من المواد كان متساوياً. وهذا تعميم لفكرة أفوجادرو التي ربطت بين عدد الجزيئات والحجم، حيث ربطت هذه الفكرة بين عدد الذرات (أو جزيئات، أيونات) والكتلة.
1911
اكتشف أينشتاين أنه قد ارتكب خطأ جبري في حساباته في أطروحة الدكتوراه، وعند تصحيحه فإنّ البيانات التجريبية نفسها ستُعطي قيمة لعدد أفوجادرو مقدارها 6.6 × 1023.
وفي هذا العام نفسه، اجتمع أينشتاين مع بيرين وبلانك وآخرون للتباحث في قضايا نظرية الكوانتم، وأخبرهم بيرين في الاجتماع بأنه وصل للبرهنة على واقعية الجزيئات.
تفسيران لمفهوم المول
طُرح تفسيران لمفهوم المول، أحدهما يرى أنّ المول وحدة كتلة كيميائية وفقًا لرؤية أوستوالد في اتصال المادة، ويملك قيم متفردة لكل نوع من الجزيئات. فمن المعروف أنّ أوستوالد عندما طرح مفهوم المول كان يهاجم فيه النظرية الذرية–الجزيئية كما مرّ سابقًا.
أما الثاني فهو يرى: أنّ المول هو عبارة عن عدد الذرات أو الجزيئات التي تؤلف (تُكوّن) المول. وهو التفسير الأكثر شيوعًا حيث يعتبر المول قيمة عددية لكمية المادة.
1929 اكتشافٌ يفتح بابًا للنقاش
تم في هذا العام اكتشاف نظيرين للأوكسجين (17O و 18O) فاقترح الفيزيائيون استخدام نظير أوكسجين-16 أساسًا لقياس الوزن الذري النسبي، بينما مقياس الكيميائيون للوزن الذري اعتمد على معدل كتلة النظائر الثلاث للأوكسجين. وبسبب هذا الاختلاف بدأت المناقشات للبحث عن نظير عنصر معياري واحد فقط لتُقاس العناصر نسبة له.
1930
في هذا العام بدأت الكتب المدرسية (textbook) الكيميائية الأمريكية في استخدام مصطلح المول. إلا أنّ استخدام المول كجزء أساسي لحل المسائل في الحساب الكيميائي لم يظهر حتى عام 1950. بل وحتى قبل عام 1961 كان يُستخدم المول للإشارة إلى كمية بعض الأشياء التي تحتوي على وحدات عدد أفوجادرو.
1959
قام الكيميائيون في (IUPAC) بتعريف المول كالآتي: عدد ذرات الأوكسجين التي يحتويها 16غ منه. أما الفيزيائيون (IUPAP) فقدموا تعريف مشابه: عدد ذرات الأوكسجين التي يحتويها 16غ من نظير الأوكسجين-16.
1960– 1961 دخول الوحدة للبراديام الذري
اتفق الطرفان IUPAC و IUPAP على التعريف التالي: المول هو كمية المادة التي تحتوي على عدد أشياء (ذرات، جزيئات …الخ) عددها مساوي لعدد الذرات الموجودة في 0.012 كغم (أو 12غ) من الكربون.”
وفي عام 1961 دخل المول رسميًا للنموذج (براديام) الذري atomistic paradigm مُمثِّلاً لكمية المادة التي تحتوي على عدد الأشياء (ذرات، جزيئات،أيونات …) مساوي لعدد الذرات التي يحتويها 12غ من نظير الكربون-12.
1967 – 1971 اقتراح اضافة الوحدة للوحدات الدولية والموافقة على ذلك
اقترحت اللجنة الاستشارية للوحدات CCU في أبريل 1967 “إضافة وحدة المول للوحدات الدولية الست الأخرى”. وفي 4 أكتوبر 1971، وافقت الـ CGPM على إضافة المول كوحدة أساسية للنظام الدولي للوحدات SI Units. وكان التعريف المعدل للمول هو عبارة عن “كمية المادة التي تحتوي على عدد منها مساوي لعدد الذرات الموجودة في 0.012 كغم من نظير الكربون-12″، وإذا تم استخدام هذه الوحدة ينبغي أن يكون عدد الأشياء محددًا، فقد تكون الأشياء ذرات أو جزيئات أو أيونات …الخ.
1980 إضافات توضيحية وعدد أفوجادرو
تم إضافة بعض الأمور التوضيحية لطبيعة الكمية التي يقيسها المول، فتم اعتبار ذرات الكربون-12 غير المتآصرة وفي حالة السكون (المستقرة) ground state أيضًا مشمولة في التعريف.
ما بعد 1980 زيادة دقة حساب عدد أفوجادرو
استمر العلماء بشتى الطرق لزيادة الدقة في حساب عدد أفوجادرو. في هذا الجدول نماذج للدقة في حساب عدد أفوجادرو مع تاريخها:
|
عدد أفوجادرو |
السنة |
|
6.0221367 × 1023 |
1986 |
|
10²³ × 6.02214199 |
1998 |
|
6.0221415 × 10²³ |
2002 |
|
10²³ × 6.02214179 |
2006 |
2018 إعادة تعريف المول وأفوجادرو
أوصت الأيوباك IUPAC في بداية عام 2018 بتعريف جديد للمول يستند على عدد محدد من الأشياء الأولية، والتعريف الجديد كالتالي:
المول وحدة دولية لكمية المادة التي تحتوي على 602,214,076,000,000,000,000,000 كيان (شيء) أولي بالضبط، وتُختصر كتابته بـ 6.02214076 ×1023، وهذه القيمة العددية ثابتة. يُطلق عليها ثابت أفوجادرو NA عندما يُعبّر عنها بوحدة mol-1، أو يُسمّى بعدد أفوجادرو بدون ذكر الوحدة.
التعريف الجديد يُشير إلى أنّ قياس كمية المادة يتعلق بعدد الأشياء بدلاً من قياس عدد الأشياء في كتلة معينة كما كان معمول في السابق.
وتم الاعتماد على التعريف الجديد للمول (وتعاريف بعض الوحدات الأخرى) من قبل CGPM في 16/11/2018 ومن المتوقع أن تدخل هذه التعاريف حيز التنفيذ في 20/05/2019 حسب ما تم نشره في موقع NIST.
القصة التي تقبع خلف تغيير تعريف المول وأفوجادرو

حسب التعريفات السابقة وبصورة مبسطة: المول هو عدد الأشياء في 0.012 كغم من نظير الكربون-12، وهذا التعريف يحتاج إلى تعريف وحدة الكيلوغرام.
والمادة التي تُعد بمثابة “وحدة الكيلوغرام” هي عبارة عن سبيكة أثرية أسطوانية الشكل من البلاتين–إيريديوم مخزونة من قبل المكتب الدولي للأوزان والمقاييس BIPM، ومشكلة هذه القطعة الأثرية أنها غير مستقرة على الأقل في المدى الطويل من الزمن. وبالتالي تغير الكتلة –ولو بصورة بسيطة– سيؤثر على دقة عدد أفوجادرو.
تخيُّل قيمة عدد أفوجادرو
عدد أفوجادرو كبير جداً بحيث يصعب تصوّره، لكن دعونا نتخيل قيمة عدد أفوجادرو ببعض الأمثلة:
- لو كان هناك كومبيوتر حديث قادر على أن يحسب (يعد) بمعدل 1 مليار في الثانية الواحدة، فإنّ هذا الأمر سيستغرق الكومبيوتر حوالي 20 مليون سنة لحساب عدد أفوجادرو!
- إذا كان لدينا مول من الثواني، أي عدد أفوجادرو من الثواني (6.02214076 ×1023 ثانية) ونحولها للسنوات لكان الناتج 4 ملايين سنة، لو كان لدينا مول واحد (عدد أفوجادرو) من كرة السلة لكان باستطاعتنا أن نُنشيء منها كوكب جديد بحجم كوكب الأرض!
- مول واحد من خلايا الدم الحمراء أكثر من خلايا الدم الحمراء لسكان الأرض الموجودين حالياً!
عدد أفوجادرو و قراءته بالصورة غير الأسية
602,214,076,000,000,000,000,000
سُتمائة واثنان سكستليون ومئتان وأربعة عشر كوانتليون وستة وسبعون كدريليون
Six Hundred and Two Sextillion, Two Hundred and Fourteen Quintillion, Seventy-Six Quadrillion
ملاحظات أخيرة على المول وعدد أفوجادرو
- ربط مفهوم المول (وحدة المول) بين الأشياء الكبيرة “العيانية” والأشياء الصغيرة “المجهرية”، مما أتاح سهولة التنقل بينهما في الحسابات العلمية، يُرمز لكمية المادة بالرمز n، ووحدة قياس كمية المادة mol، ولعدد أفوجادرو NA.
- لأجل الدقة، عندما نقول ثابت أفوجادرو نتبعه بذكر الوحدة mol-1، وعندما نقول عدد أفوجادرو نذكر العدد فقط بدون وحدة.
المصادر:
- The Mole Concept in Chemistry, Kieffer, W. F. 1965.
- Mole, Doris Kolb, Journal of Chemical Education
- A History of Chemistry, Partington, J. R., vol.4, p. 217
- The Chemistry Book “From Gunpowder to Graphene, 250 Milestones in The History of Chemistry”, Derek B. Lowe
- Jensen, (2004), The Origin of the Mole Concept, Journal of Chemical Education, 81(10), 1409.
- Quantities, Units and Symbols in Physical Chemistry, 3ed, IUPAC
- Atomic Weight’ -The Name, Its History, Definition, and Units, IUPAC, 1992.
- Guide for the Use of the International System of Units (SI), NIST, 2008.
- General Chemistry, Principles and Modern Applications, Ralph H, Petrucci and others , 3ed.
- The Avogado experiment and the redefinition of the mole – an SI-unit for chemistry, Dr: Bernd Güttle.
- Padilla, K., & Furio-Mas, C, (2007), The Importance of History and Philosophy of Science in Correcting Distorted Views of “Amount of Substance” and “Mole” Concepts in Chemistry Teaching. Science & Education, 17(4), 403–424.
- Brownian Movement and Molecular Reality, J, Perrien, 1910.
- Cerruti, L (1994), The Mole, Amedeo Avogadro and Others, Metrologia, 31(3), 159–166.
- Mole Concept, Chemistry Explained, Retrieved December 17, 2018, from http://www.chemistryexplained.com/Ma-Na/Mole-Concept.html
- The Mole and History of The Term “Mole”, Kent Chemistry, Retrieved December 17, 2018, from http://www.kentchemistry.com/links/GasLaws/Mole.htm
- A NEW DEFINITION OF THE MOLE HAS ARRIVED, IUPAC, Retrieved December 17, 2018, from https://iupac.org/new-definition-mole-arrived/ How big is a mole? TED-Ed Blog, Retrieved December 17, 2018, from https://blog.ed.ted.com/2013/10/23/how-big-is-a-mole-exactly/
- Mole (unit), Academic Kids, Retrieved December 17, 2018, from http://academickids.com/encyclopedia/index.php/Mole_%28unit%29
- Avogadro’s number, Citizendium, Retrieved December 17, 2018, from http://en.citizendium.org/wiki/Avogadro%27s_number
- A new definition of the mole, Chemistry World, Retrieved December 17, 2018, from https://www.chemistryworld.com/opinion/a-new-definition-of-the-mole/3008663.article
- Redefining the Mole. NIST. Retrieved December 17, 2018, from https://www.nist.gov/si-redefinition/redefining-mole