دراسة تكشف حجم الجزيئة الأمثل للأدوية النانومترية المضادة للسرطان

ترجمة: ريم أبو عاصي، الكيمياء العربي
ترتكز الأدوية النانومترية على جزيئاتها النانومترية والتي تعمل على إيصال الدواء بشكل مُستهدِف لأنسجة معينة أو خلايا محددة وبذلك تَنتُج لدينا منظومة حلولٍ جديدة لتشخيص وعلاج مرض السرطان. ويُعدّ العمل على فهم الترابط بين الخواص الفيزيوكيميائيةللأدوية النانومترية وعلاقة تلك الخواص بالاستجابات والوظائف الحيوية أمراً أساسياً لتطوير هذه المنظومة كمضاد فعّال لمرض السرطان.
يقول الدكتور جاينجون شينغ الأستاذ المساعد في قسم الهندسة وعلوم المادة، جامعة إلينوس منطقة أوربانا – شامبينغ،”إنّ العمل على تطوير جيل جديد من الأدوية النانومترية قادرٍ على تحمل صفاتٍ أكثرَ شمولاً في مجال أمراض السرطان إنما يتطلب منّا أن نفهم ترابط العلاقة بين صفات تلك الأدوية الفيزيوكيمائية، خاصة حجم الجزيئة، وتأثيرها على الأجهزة الحيوية”.
وفي دراسة حديثة تم نشرها في الوقائع الأكاديمية الوطنية للعلوم قام البروفيسور شينغ Jianjun Cheng وزملاؤه بتقييم مركزي ممنهج لمقدار اعتماد الخواص الحيوية على الأحجام النانومترية من خلال مراقبة ثلاثة أحجام مختلفة لمركبات أحادية الانتثار والتي صُنّعت على شكل معقدات نانوية من صنف دواء_ سيليكا و ضمن مدى أحجام 20،50، 200 نانومتر.
يضيف البروفيسور شينغ: ” لقد شهدنا إندفاعاً كبيراً نحو المزيد من تصغير حجم الجزيئات النانومترية باستخدام الكيمياء الحديثة والتصميم الهندسي، لكن في الواقع، يترواح مقاس حجم الجزيئة لأحدث دواء مضاد للسرطان تمت الموافقة عليه مابين 100 -200 نانومتر، بينما تكشف الدراسات المخبرية على الحيوانات بأنّ أدوية مضادة للسرطان ذات أحجام جزيئة أصغر وتحديداً 50 نانومتر فأقل، تُظهر أداءاً أكثر فاعلية من ناحية تغلغلٍ أكبر في الأنسجة وتثبيطٍ أفضل للورم”.
ويعلّق الكاتب الأساسي للمقال الذي نُشر في الوقائع الأكاديمية الوطنية للعلوم، الباحث لي تانغ Li Tang: “خلال العقود الثلاث المنصرمة، ساد إجماع على أن لحجم الجزيئة دور محوري في تحديد التوزع الحيوي، التغلغل في الورم، الدمج الخلوي، التصفية من مصل الدم والأنسجة، إضافة لعملية الإطراح من الجسم، وكلها تُعد عواملاً مؤثرةً على الكفاءة العلاجية الشاملة لأمراض السرطان. إنّ الدراسة التي قُمنا بها إنما هي دليلٌ قاطع على أن هناك أحجاماً جزيئة مُثلى للأدوية النانومترية المضادة للسرطان، ومن خلال الوصول لتلك الأحجام يحدث الاحتواء الأكبر للورم”.
[fusion_builder_container hundred_percent=”yes” overflow=”visible”][fusion_builder_row][fusion_builder_column type=”1_1″ background_position=”left top” background_color=”” border_size=”” border_color=”” border_style=”solid” spacing=”yes” background_image=”” background_repeat=”no-repeat” padding=”” margin_top=”0px” margin_bottom=”0px” class=”” id=”” animation_type=”” animation_speed=”0.3″ animation_direction=”left” hide_on_mobile=”no” center_content=”no” min_height=”none”]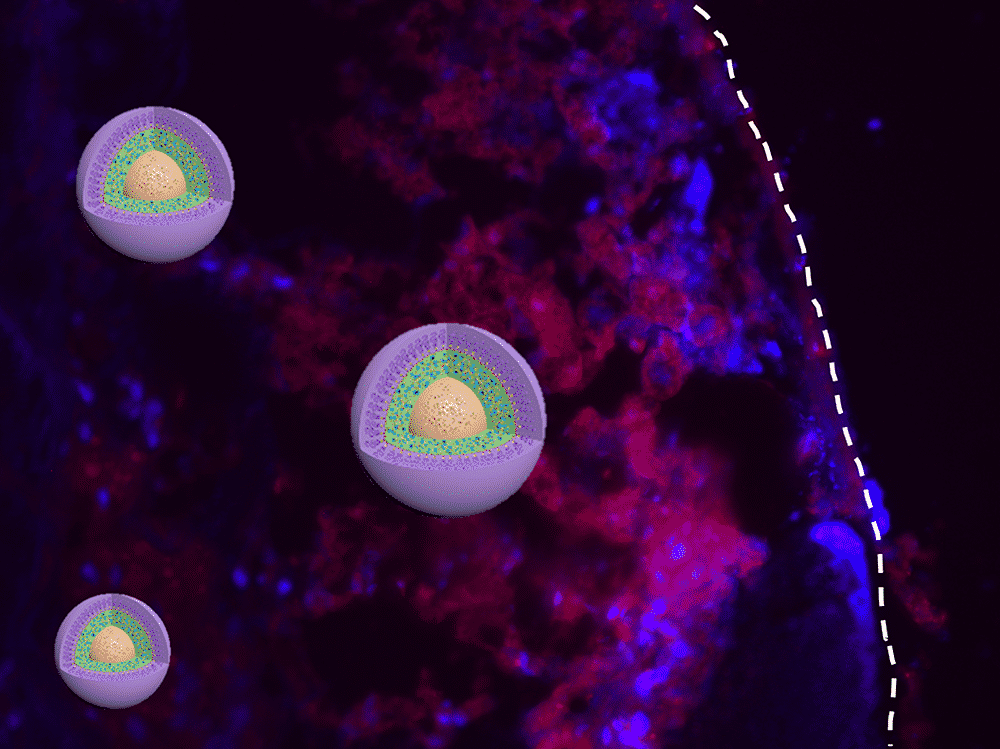
من ضمن مجموعة المعقدات النانومترية التي تم التحقق منها، أظهرت المعقدات ذات الحجم 50 نانومتر مزيجاً لأكثر الخواص مثاليةً، كالتغلغل العميق في الأنسجة الورمية، والدمج الفعال للخلايا السرطانية بالإضافة للقدرة على التصفية البطيئة للورم، مُظهرةً فعاليتها العليا على الأورام الأولية والأورام النقلية في إطار مرحلة التجارب المخبرية الحيوانية.
في الختام أشار البروفيسور شينغ إلى أنّ العلماء قد طوروا نموذجاً حسابياً للتوزع المكاني-الزماني للجزيئات النانومترية ضمن ورم متماثل كروياً وذلك بهدف المضي قُدماً نحو تطوير رؤية حقيقية عن علاقة حجم الجزيئة في الأدوية النانومترية واعتماد ذلك على قدرة الدواء في التراكم داخل الورم و من ثم احتوائه. أما نتائج هذا البحث فقد كانت فائقة الأهمية لتوجيه الباحثين المستقبلين نحو تصميم أدوية نانومترية جديدة لعلاج أمراض السرطان.
إضافة لذلك، فقد نجح فريق من الباحثين في جامعة إيلينويس بتطوير دواء نانومتري جديد مصمم بدقة حجمية عالية ضمن المدى الحجمي الأمثل والقادر على تثبيط سرطان الثدي عند الإنسان، ومنع النمو الخبيث للورم في الحيوانات، لتكون هذه النتائج أملاً واعداً لعلاج أنواع عدة من السرطانات.
المصدر:
Study reveals optimal particle size for anticancer nanomedicine. (n.d.). Retrieved November 16, 2014, from http://engineering.illinois.edu/news/article/9546
Study reveals optimal particle size for anticancer nanomedicines
10/15/2014
Author: Jianjun Cheng, Department of Materials Science and Engineering, University of Illinois at Urbana-Champaign.
Tel: +1 217-244-3924.
Translator: Reem Abou Assi, Department of pharmaceutical technology and drug delivery, Pharmacy school at University of Science Malaysia.
Twitter: @remose1383.


